Плоскоклеточный рак кардиального отдела желудка

Кардия, или кардиальный отдел желудка, представляет собой цилиндрический сегмент, охватывающий пищеводно-желудочный переход и пространство на 2 см выше и ниже его. Рак кардиального отдела желудка (кардиоэзофагеальный рак, КЭР) отличается анатомическими и клиническими особенностями, и требует особого подхода в лечении. Многие эксперты даже выделяют его в отдельную нозологию, и на это есть несколько причин:
- Опухоли данной локализации склонны распространяться на пищевод гораздо чаще, чем рак нижележащих отделов желудка.
- Такие опухоли метастазируют в абдоминальные и медиастинальные лимфоузлы.
- Кроме того, они отличаются более неблагоприятным прогнозом, чем рак желудка или пищевода.
Для кардиоэзофагеального рака характерны агрессивный рост и склонность к метастазированию в лимфатические узлы средостения.
Причины
Причины развития рака кардиального отдела достоверно неизвестны. В настоящее время принято говорить о факторах риска – обстоятельствах, при которых увеличивается вероятность развития той или иной патологии. При раке желудка они следующие:
- Инфицирование Helicobacter pylori.
- Наличие атрофического гастрита проксимальных отделов желудка.
- Наследственная предрасположенность.
- Курение и злоупотребление алкоголем.
Что касается гастроэзофагеального рефлюкса и пищевода Баррета, то эти состояния – главные предрасполагающие факторы развития эзофагеального рака, но они не влияют на частоту развития рака кардии.
Симптомы рака кардиального отдела желудка
Для рака кардии наиболее характерны снижение веса, отвращение к пище, боль и дисфагия. Боль обычно локализуется в области эпигастрия, носит постоянный, давящий характер и не зависит от приема пищи. Иногда она отдает в поясничную область или за грудину. В последнем случае болезнь может симулировать патологию сердца, например стенокардию.
Степень выраженности дисфагии зависит от размеров опухоли и обструкции пищеварительного тракта. В основном она проявляется нарушением питания, которое приводит к гиповолемии и изменению баланса электролитов.
Классификация
Классификация рака кардии ориентируется на локализацию центра опухоли. Точкой анатомического отсчета является Z-линия – линия пищеводно-желудочного перехода.
- Рак I типа – центр новообразования располагается на расстоянии 1-5 см выше Z-линии в сторону пищевода.
- Рак II типа – центр новообразования располагается в пределах 1 см орально и 2 см ниже Z-линии.
- Рак III типа – центр новообразования располагается на расстоянии 2-5 см ниже Z-линии.
Диагностика
- Эндоскопическое исследование желудка и пищевода. Позволяет осмотреть опухоль и взять биопсию для морфологического исследования.
- Эндоскопическое УЗИ. Проводится для определения степени инвазии опухоли, ее прорастания в соседние органы и структуры, а также для поиска регионарных метастазов.
- Абдоминальное УЗИ. Проводится для поиска метастазов.
- Рентгеноконтрастное исследование. Позволяет определить протяженность опухоли и оценить степень стеноза кардии и пищевода. Особенно актуален метод при диффузно-инфильтративных формах рака, когда из-за подслизистой локализации могут быть получены ложноотрицательные результаты биопсии.
- КТ – проводится для поиска отдаленных метастазов.
- Диагностическая лапароскопия. Позволяет обнаружить распространение опухоли на серозные оболочки, а также диагностировать интраперитонеальную диссеминацию.
- Определение онкомаркеров – РЭА, СА 19-9, СА 72-4.
Лечение рака кардиального отдела желудка
Лечение рака кардии требует комбинированного подхода и включает химиотерапию и операцию. При нерезектабельных опухолях основной метод лечения – химиотерапия, а операции выполняются по жизнеугрожающим показаниям.
Оперативное лечение
Выбор объема операции и оперативного доступа определяется исходя из типа рака и его местной распространенности. При КЭР I типа проводят проксимальную резекцию желудка
КЭР I типа Проксимальная резекция желудка, субтотальная резекция пищевода. | КЭР II типа Гастрэктомия (удаляется весь желудок), резекция нижнегрудного отдела пищевода | КЭР III типа Гастрэктомия, резекция нижнегрудного отдела пищевода. |
Минимальный объем лимфодиссекции подразумевает удаление лимфатических узлов 1 и 2 порядка (проводится расширенная лимфодиссекция в объеме D2). При КЭР I проводится билатеральная медиастинальная лимфодиссекция.
Химиотерапия
Химиотерапия проводится по одному из следующих вариантов:
- Периоперационная химиотерапия. Выполняется в режиме CF или ECF на протяжении 8-9 недель до операции и после.
- Адъювантная химиотерапия. Ее начинают через 4-6 недель после операции, если не было тяжелых осложнений, и проводят в течение 6 месяцев. Применяют схемы XELOX или CAPOX.
- Адъювантная химиолучевая терапия. В настоящее время применяется редко и только в случае нерадикальной операции.
Лечение нерезектабельных и диссеминированных опухолей проводится с помощью химиотерапии по схемам CF, CX, XELOX в режиме 6-8 трехнедельных курсов, или 9-12 двухнедельных курсов. После этого лечение прекращают и проводят наблюдение до прогрессирования заболевания. При HER2-положительном раке желудка возможно проведение терапии трастузумабом.
После прогрессирования заболевания химиотерапию возобновляют, схему лечения подбирают с учетом имеющегося анамнеза.
Метастазирование
При КЭР I и II типа метастазирование главным образом происходит в лимфатические коллекторы паракардиальной зоны, чревного ствола и малой кривизны желудка. При КЭР I типа в процесс могут вовлекаться и медиастинальные узлы. Такие особенности метастазирования учитываются при планировании операции и лимфодиссекции.
Осложнения и рецидивы
Главные осложнения кардиоэзофагеального рака:
- Распад опухоли и кровотечения. В этом случае требуется неотложное эндоскопическое обследование и остановка кровотечения. Если эндоскопически проблему решить не удалось, проводят хирургическое вмешательство.
- Опухолевый стеноз. Это осложнение приводит к дисфагии и, как следствие, к развитию алиментарных нарушений. Для его устранения применяются реканализация, баллонная дилятация, стентирование. В тяжелых случаях показано наложение обходного анастомоза или выведение гастростомы.
- Боль. Для уменьшения болевого синдрома применяют лучевую терапию, медикаментозное лечение и в ряде случаев локорегионарную анестезию.
- Асцит – скопление жидкости в брюшной полости. Для его устранения назначают диуретики и внутриполостную химиотерапию. При скоплении больших объемов жидкости показан лапароцентез – эвакуация содержимого посредством пункции.
Прогноз и профилактика
5-летняя выживаемость при КЭР любого типа в среднем составляет 23,6%. Наиболее неблагоприятно протекают опухоли III типа, поскольку они преимущественно представлены низко- или недифференцированными новообразованиями. 5-летняя выживаемость при данной локализации составляет около 14%. Существенно ухудшает прогноз наличие метастазов в лимфоузлах средостения.
В Европейской клинике работают врачи с большим опытом лечения рака желудка. Мы руководствуемся актуальными европейским стандартами. Для этого в клинике имеется все необходимое – от новейших лекарственных препаратов до современного оборудования, благодаря чему мы готовы оказать помощь в самых тяжелых случаях.
Источник
Карцинома желудка – это рак и второй по частоте из всех злокачественных опухолей, ежегодно он поражает почти 36 тысяч россиян. За последнее десятилетие заболеваемость существенно снизилась, но доля женщин возросла. Сегодня на четырёх больных мужчин приходится три женщины. В большинстве случаев болезнь развивается у переживших 50-летие.
Причины возникновения и факторы риска
Причины злокачественного новообразования слизистой желудка окончательно не выяснены.
Несомненна роль генетической предрасположенности в сочетании с определённой моделью питания, поскольку опухолевый процесс часто поражает целые народы: японцев, чилийцев, китайцев и корейцев. Американцы и австралийцы, наоборот, болеют нечасто. Россияне тяготеют к группе часто болеющих.
Замечено повышение частоты желудочной карциномы у долго страдающих атрофическим или гиперпластическим гастритом и некоторыми видами полипов, в инициации которых замечена хеликобактерная инфекция – заражение бактерией H.Pylori.
К несомненным факторам риска рака отнесена резекция желудка по поводу любого заболевания. Связь карциномы с язвой желудка совсем не очевидна. Пока больше данных за то, что язва не перерождается в рак, а на ранних этапах един механизм образования патологии слизистой оболочки и некоторые формы рака внешне неотличимы от язвы, поэтому разобраться «что есть что» можно только с помощью биопсии.
Часто новообразование развивается при длительном дефиците витамина В12, как правило, проявляющемся специфической пернициозной анемией и гастритом.
Не доказана пагубная роль вредных привычек – курения и употребления алкоголя, но они способствуют развитию фоновых процессов, к коим причислены все выше описанные заболевания желудочной слизистой.
Симптомы желудочной карциномы
Ранние стадии рака вызывают такие же симптомы, что и любая доброкачественная или воспалительная патология желудочно-кишечного тракта, не вынуждая испытывающего дискомфорт человека обратиться к врачу.
Зачастую вообще нет ни единого признака недуга, поэтому так важно при фоновых процессах регулярно выполнять эндоскопическое обследование ЖКТ.
Желудок растягивается, маскируя уменьшение своей вместимости растущей опухолью, а симптомы не отличаются от банального обострения хронического гастрита, насторожить может только прогрессирующая потеря массы тела при увеличении объёма живота – свидетельство канцероматозного обсеменения брюшной полости с образованием асцита.
Боли типичны для язвы, при раке желудка боли возникают, когда в опухолевый конгломерат запаиваются нервные стволы брюшной полости или вовлекаются соседние органы. Больше половины больных замечают признаки распространённого злокачественного процесса:
- снижение веса,
- увеличение размера живота,
- рвоту после еды,
- появление лимфатических узлов над ключицей или прощупывая уплотнение в подложечной области.
Классификация и разновидности
По клеточному строению подавляющая доля новообразований желудка представлена аденокарциномой, что характерно для всего желудочно-кишечного тракта. Возможны морфологические варианты в виде папиллярной или тубулярной, муцинозной или перстневидно-клеточной аденокарциномы.

Выбор оптимального метода лечения базируется не столько на клеточной разновидности, сколь на степени её агрессивности, то есть дифференцировке, где минимальная обозначается как «высокодифференцированная». Высокая злокачественность присуща низкодифференцированной форме.
Инвазивная карцинома желудка не отдельная болезнь, это естественный процесс развития опухоли, когда она уже не изолированная колония раковых клеток на отдельном участке слизистой оболочки, а внедряется в окружающие ткани, разрушая всё мешающее для её продвижения вглубь и вширь, и обрела способность к метастазированию.
Стадии развития карциномы желудка
Стандартно рак градуируют по стадиям TNM – от первой до четвёртой. Каждой стадии присущ определённый размер первичного очага, который обозначают литерой «Т», и степень вовлечения лимфатических узлов брюшной полости – литера «N». С I по III стадии включительно метастазы в другие органы исключены, то есть «М» всегда только 0.
Схематично и упрощённо стадии трактуются следующим образом:
- Начальные этапы развития, когда раковые клетки не проникли дальше слизистой оболочки, обозначают как ранний рак желудка, то есть карцинома первой стадии или меньше – in situ.
- Метастазы в лимфатические узлы даже при крошечной опухоли, как минимум, вторая стадия.
- Выход карциномы через желудочную стенку в брюшную полость – третья стадия.
- Метастазы рака в другие органы – четвертая.
Профилактика
Профилактика возможна только при ясности причин, приводящих к карциноме. Сегодня онкологам известен список заболеваний, при которых повышена вероятность развития новообразования в слизистой оболочке, но сама первопричина злокачественного перерождения неизвестна.
Профилактика ограничена лечением фоновых болезней желудка и регулярным наблюдением за течением доброкачественных процессов. Ведущий способ скрининга – гастроскопия, позволяющая оценить состояние слизистой оболочки и взять её на анализ.
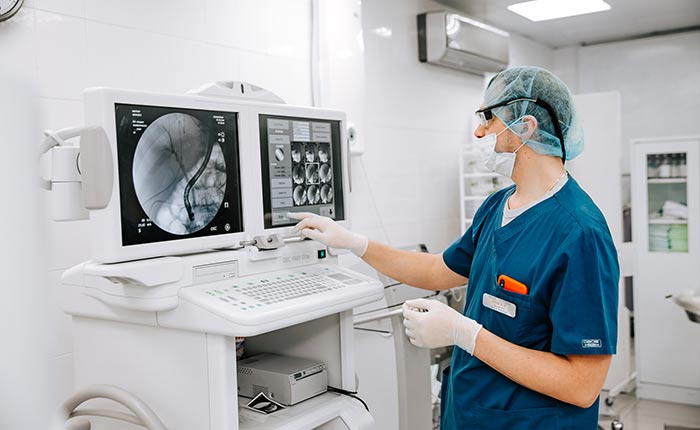
Для пациентов, перенесших первичное лечение желудочной карциномы, профилактика – это регулярное обследование для раннего обнаружения рецидива опухоли и метастазов.
Диагностика
- Наиболее информативна эндоскопия – эзофагогастроскопия, позволяющая сразу взять для исследования не менее 6 кусочков повреждённой ткани.
- Дополнение гастроскопии УЗИ-исследованием – эндосонография достаточно чётко определит глубину проникновения ракового процесса в желудочную стенку.
- Протяженность поражения стенок органа выясняется при полипозиционном рентгеноконтрастном исследовании.
- КТ брюшной полости выявит метастазы в лимфатической системе и уточнит вовлечение в злокачественный процесс окружающих тканей и органов.
- Обязательное исследование перед операцией – лапароскопия, при которой выявляют канцероматоз брюшины.
Методы лечения и прогнозы
Хирургическое вмешательство при желудочной карциноме – единственный метод радикального лечения. Сегодня предпочтение отдано операциям, позволяющим максимально сохранить органы при безоговорочном удалении всех очагов рака.
Лапароскопические вмешательства по результатам равноценны классическому подходу и позволяют сократить период восстановления.
При раннем раке проводится небольшая эндоскопическая операция, 99% пациентов живут долго и без онкологических проблем.
При первой-второй стадии выполняется резекция. Подавляющее большинство больных с маленькой опухолью проживёт 5 – 10 лет без рецидива заболевания, при второй стадии 5 лет переживает почти две трети оперированных.
При распространении рака за пределы желудка и возможности удаления всего ракового конгломерата проводятся комбинированные операции, включающие резекцию части органа или полное удаление – гастрэктомию. К сожалению, вероятность развития рецидива в этой стадии болезни достаточно высока, поэтому через месяц-полтора после операции начинается профилактическая химиотерапия, длящаяся не менее полугода.
При отсутствии отдалённых метастазов, но технически невозможном удалении опухолевого конгломерата, на первом этапе около 9 недель делают химиотерапию, что в части случаев позволяет выполнить отсроченную операцию, дополняемую в дальнейшем профилактической ХТ. При отсутствии позитивных изменений на фоне лекарственной терапии возможна локальная лучевая терапия, как правило, вместе с изменением схемы химиотерапии.
При метастазах в другие органы операция не показана, хирургическая помощь оказывается только при опасных для жизни осложнениях: кровотечении, фатальном сужении выхода из желудка или перфорации с развитием перитонита. Основной метод лечения – химиотерапия.
При карциноме желудка, как ни при каких других процессах, несомненна высока потребность в паллиативной помощи, в том числе и хирургического плана. Симптоматическая терапия повышает скорость восстановления после операции и химиотерапии, значимо улучшает самочувствие и помогает пациенту с метастазами жить дольше и активнее. В Европейской клинике каждый больной получает не просто оптимальную помощь, но лечение класса «всё самое лучшее из известного».
Список литературы
- Бондарь Г.В., Попович А.Ю., Сидюк А.В. и соавт./ Сравнение различных методов химиотерапии при метастатическом нерезектабельном раке желудка // Новообразование, 2013, Т. 6.; № 1 (12).
- Гусейнов А.З., Истомин Д.А., Гусейнов Т.А./ Объем оперативных вмешательств при раке желудка: современные тенденции // Вестник новых медицинских технологий, 2013, № 1.
- Каприн А.Д., Соболев Д.Д., Хомяков В.М., и соавт. /Результаты комбинированного лечения больных местно-распространенным и диссеминированным раком желудка с использованием гипертермической интраоперационной внутрибрюшной химиотерапии // Онкология, 2014, Т.2; № 6.
- Indrakumar A., Mandakulutur S.G., Baara R.K. /Role of staging laparoscopy in upstaging CT findings and influencing treatment decisions in gastric cancers // Int J Res Med Sci., 2016; 4(12).
- Koppe M.J., Boerman O.C., Oyen W.J., et al. /Peritoneal carcinomatosis of colorectal origin: incidence and current treatment strategies// Ann Surg 2006; 243.
Источник
Рак пищевода – злокачественное заболевание, исходящее из его слизистой оболочки. Рак является наиболее частым заболеванием пищевода. Болеют преимущественно мужчины (3:1), у женщин рак пищевода не входит в список 10 наиболее распространённых онкологических заболеваний. Учитывая анатомическую структуру пищевода, самой частой формой рака пищевода в мире является плоскоклеточный рак.
На втором месте – аденокарцинома пищевода – рак, исходящий из железистого эпителия.
Анатомия пищевода
Пищевод представляет собой полую мышечную трубку, которая соединяет глотку и ротовую полость с желудком. Стенка пищевода построена из слизистой оболочки, подслизистой основы, мышечной и адвентициальной оболочек. Мышечная оболочка пищевода состоит из двух слоев: наружного продольного и внутреннего циркулярного. В верхней части пищевода мышечная оболочка образована поперечно-мышечными волокнами. Примерно на уровне одной трети пищевода (считая сверху) поперечно-полосатые мышечные волокна постепенно заменяются гладкомышечными. В нижней части мышечная оболочка состоит только из гладкомышечной ткани.
Слизистая оболочка покрыта многослойным плоским эпителием, в подслизистой оболочке находятся слизистые железы, открывающиеся в просвет органа.
В пищеводе слизистая оболочка кожного типа. Эпителий многослойный плоский неороговевающий, лежит на тонковолокнистой соединительной ткани – собственном слое слизистой оболочки, состоящем из тонких пучков коллагеновых волокон; содержит также ретикулиновые волокна, соединительнотканные клетки. Собственный слой слизистой оболочки вдаётся в эпителий в виде сосочков.
Особенностью пищевода является отсутствие у него серозной оболочки, наружной слой представлен адвентицией, рыхлой соединительной тканью. Лишь в нижней трети пищевод, точнее его абдоминальный отдел, покрыт серозой.
Распространенность рака пищевода
Примерно 80% всех случаев рака пищевода диагностируются в развивающихся странах, где доминирующей гистологической формой является плоскоклеточный рак. В то же время аденокарцинома, за редким исключением, встречается только в индустриально развитых странах.
Для заболеваемости раком пищевода характерна выраженная географическая вариабельность со 100- и более кратной разницей между высшими и низшими показателями. Самая высокая заболеваемость (>150) отмечена в Иране и других странах т.н. Каспийского пояса, а именно, в некоторых районах Туркменистана и Казахстана, прилегающих к Каспийскому морю, а также в Каракалпакии, причем в этих эндемических по раку пищевода регионах заболеваемость высока как среди мужчин, так: и среди женщин. Заболеваемость раком пищевода в Муйнакском районе Каракалпакии составляет 126 – среди мужчин и 150 – среди женщин. Другие очаги высокой заболеваемости – некоторые регионы Китая. Высокая заболеваемость отмечается также в Зимбабве среди чернокожих мужчин (19). В развитых странах относительно высокая заболеваемость раком пищевода (>10) регистрируется во Франции (Кальвадос -17) и в США среди чернокожих мужчин (11).
В России заболеваемость раком пищевода относительно невысока и сравнима с аналогичными показателями в других странах Европы. Однако в некоторых регионах, например в Якутии, заболеваемость раком пищевода значительно выше. Очень высокая частота развития рака пищевода (более 150) отмечается среди малочисленных народов Севера и Дальнего Востока России. Смертность от рака пищевода коррелирует с показателями заболеваемости и имеет те же географические особенности.
Заболеваемость раком пищевода снижается в большинстве стран мира, в том числе и в России. Однако в ряде развитых стран за последние годы наметился рост заболеваемости аденокарциномой кардиального отдела пищевода, которая, но данным ряда канцер-регистров, составляет более 50% всех случаев рака пищевода.
При раке пищевода 5-летняя выживаемость колеблется в пределах 5-12% и остается без изменения в течение двух десятилетий.
Причины и факторы риска
Этиология рака пищевода имеет региональные особенности, а также зависит от локализации и гистологического типа опухоли. Основными факторами риска плоскоклеточного рака пищевода в развитых странах являются курение табака и чрезмерное потребление алкогольных напитков. Для аденокарциномы кардии, наряду с этими двумя факторами, важное значение имеет гастроэзофагеальный рефлюкс, который приводит к постоянному раздражению и повреждению слизистой оболочки кардии, ее метаплазии и дисплазии.
Этиология рака пищевода в регионах с очень высокой заболеваемостью до конца не ясна. Скорее всего, очень высокий риск развития рака пищевода в эндемических регионах, а именно в Иране, Центральной Азии и Китае, связан с дефицитом овощей и фруктов и, соответственно, витаминов и других микроэлементов в питании. Кроме того, предполагают, что риск развития рака пищевода повышен в связи с употреблением очень горячих напитков – чая в Иране и Центральной Азии и мате – в Южной Америке. Высказаны предположения о возможной роли орального потребления некоторых форм табака, например бетеля, а также опия. Рассматривается роль ВПЧ и загрязнения продуктов питания канцерогенными грибами.
Развитее плоскоклеточного рака пищевода связано также с другими его заболеваниями, такими как:
- стриктуры (сужение пищевода) на фоне употребления агрессивных жидкостей или длительного пищеводно-желудочного рефлюкса,
- ахалазия кардии,
- склеродермия,
- синдром Пламмера-Вильсона (развитие пищеводных мембран у женщин с железодефицитный анемией).
У пациентов с таким заболеванием как гиперкератоз (ладоней и стоп), имеющего аутосомно-доминантный тип наследования, к 45 годам плосколеточный рак пищевода развивается у 50% больных, а к 55 годам – у 95%.
Рак пищевода симптомы
Ранние формы рака протекают бессимптомно, поскольку для появления затруднения проглатывания пищи (дисфагии) необходимо сужение просвета пищевода менее 15 мм.
К сожалению, более половины пациентов (60%) к моменту установления диагноза имеют распространённую стадию заболевания.
Основными симптомами при раке пищевода являются:
- Дисфагия.
- Боли при проглатывании пищи.
- Спрыгивание съеденной пищей (регургитация).
- Боли и дискомфорт в грудной клетке.
- Чувство инородного тела в пищеводе.
- Осиплость голоса (при вовлечении в процесс возвратного гортанного нерва).
- Появление увеличенных лимфоузлов на шее.
- Снижение массы тела.
Для плоскоклеточного рака характерно развитие местно-распространённого процесса с вовлечением в опухоль прилегающих жизненно-важных анатомических структур, таких как аорта, трахея, главные бронхи, сердце.
Метастазирование плоскоклеточного рака пищевода происходит лимфогенным путём с развитием отдалённых метастазов в печени, легких, костях.
Диагностика
- Основными диагностическими инструментами у больных плоскоклеточным раком пищевода является рентгенография пищевода с барием (выявление злокачественной стриктуры пищевода, ее протяженности и степени сужения пищевода) и эндоскопическое исследование пищевода и желудка с проведением биопсии новообразования.
- С целью установления стадии заболевания, исключения отдалённых метастазов и оценки местной распространенности процесса необходимо проведение МСКТ органов грудной клетки и брюшной полости с внутривенным контрастированием.
- С целью оценки глубины инвазии опухоли проводят эндосонографическое эндоскопическое исследование (одномоментное проведение эндоскопии и ультразвукового исследования).
- У больных с раком пищевода средней трети необходимо проведение фибробронхоскопии для исключения вовлечения в опухолевый процесс трахеи и главных бронхов.
- ПЭТ/КТ (с 18F-дезоксиглюкозой) мало информативна для определения состояния первичной опухоли (Т) и регионарных лимфатических узлов (N), но по сравнению с КТ демонстрирует более высокую чувствительность и специфичность в обнаружении отдаленных метастазов; ПЭТ/КТ рекомендуется выполнять в том случае, если у пациента нет отдаленных метастазов по данным КТ.
Классификация
Плоскоклеточный рак пищевода как и все злокачественные опухоли классифицируют и стадируют в соответствие с международной классификацией TNM (8-ой пересмотр).
Система стадирования рака пищевода по TNM (UICC, 8‐е издание)
Первичная опухоль
Тх Первичная опухоль не может быть оценена;
Т0 Нет признаков первичной опухоли;
Tis Карцинома in situ/дисплазия высокой степени;
Т1 Прорастание опухоли в собственную пластинку или подслизистый слой;
Т1а Опухоль вовлекает собственную пластинку или мышечную пластинку слизистой оболочки Т1b Опухоль прорастает подслизистый слой;
Т2 Прорастание мышечного слоя;
Т3 Прорастание адвентиции;
Т4 Прорастание прилегающих структур;
Т4а Плевра, брюшина, перикард, диафрагма, вена azygos;
Т4b Прилежащие анатомические структуры: аорта, позвонки, или трахея.
Регионарные лимфатические узлы
Nx Регионарные лимфатические узлы не могут быть оценены;
N0 Нет метастазов в регионарных лимфатических узлах;
N1 Поражение 1-2 регионарных лимфатических узлов;
N2 Поражение 3-6 регионарных лимфатических узлов;
N3 Поражение 7 и более регионарных лимфатических узлов.
Отдаленные метастазы
М0 Отдаленных метастазов нет;
М1 Отдаленные метастазы есть.
Регионарными являются следующие группы лимфатических узлов:
- прескаленные;
- внутренние яремные;
- верхние и нижние шейные;
- шейные околопищеводные;
- претрахеальные (билатеральные);
- лимфатические узлы корня легкого (билатеральные);
- верхние параэзофагеальные (выше v. azygos);
- бифуркационные;
- нижние параэзофагеальные (ниже v. azygos);
- задние медиастинальные;
- диафрагмальные;
- перигастральные (правые и левые кардиальные, лимфатические узлы, вдоль малой кривизны, вдоль большой кривизны, супрапилорические, инфрапилорические, лимфатические узлы вдоль левой желудочной артерии).
Категория pN0 может быть установлена только после лимфодиссекции с патоморфологическим изучением не менее 7 удаленных лимфоузлов (при отсутствии в них метастазов).
Рак пищевода лечение
Основным методом лечения является хирургический. Лишь при невозможности хирургического лечения (отказ пациента или функциональные противопоказания) проводится химиолучевая терапия в самостоятельном варианте.
При росте опухоли в пределах слизистой оболочки (T1) возможно выполнение эндоскопической резекции в пределах слизистой оболочки или подслизистого слоя. Эндоскопическая резекция является методом выбора при РП in situ и при тяжелой дисплазии. Кроме того, метод успешно применяется при опухолях пищевода, не выходящих за пределы слизистой оболочки, у больных, имеющих значительный риск хирургических осложнений. При этом 5-летняя выживаемость достигает 85-100%.
Виды операций
- Основным видом операции при РП является трансторакальная субтотальная резекция пищевода с одномоментной внутриплевральной пластикой стеблем желудка или сегментом толстой кишки с билатеральной двухзональной медиастинальной лимфодиссекцией из комбинированного лапаротомного и правостороннего торакотомного доступов (операция типа Льюиса).
- При локализации опухоли в верхнегрудном или шейном отделах возможно выполнение трансторакальной резекции пищевода с анастомозом на шее (операция типа Мак Кейна).
- В некоторых клиниках в качестве альтернативы выполняются трансхиатальные резекции пищевода, которые не могут претендовать на радикальность. Они не должны применяться у пациентов раком грудного отдела пищевода, поскольку из лапаротомного доступа невозможна адекватная медиастинальная лимфодиссекция выше бифуркации трахеи.
- Другим путем уменьшения частоты хирургических осложнений является минимально инвазивная (торако-лапароскопическая) или гибридная (торакотомия + лапароскопия или торакоскопия + лапаротомия) эзофагэктомия или роботассистированная резекция пищевода.
Выбор метода хирургического лечения при опухоли пищеводно-желудочного перехода определяется ее локализацией согласно классификации Зиверта:
- при I типе выполняется операция Льюиса или операция Гэрлока в зависимости от размеров опухоли, в исключительных случаях (при невозможности торакотомии) – трансхиатальная резекция пищевода;
- при II типе выполняется чресплевральная проксимальная резекция (операция Гэрлока) либо чрезбрюшинная проксимальная резекция с широкой диафрагмотомией и высоким анастомозом в средостении (у соматически отягощенных больных);
- при III типе выполняется чрезбрюшинная проксимальная резекция или гастрэктомия.
При клинической стадии II-III вариантами лечения являются:
- предоперационная ХТ + хирургическое лечение;
- предоперационная химиолучевая терапия + хирургическое лечение;
- хирургическое лечение;
- самостоятельная химиолучевая терапия.
Химио и лучевая терапия
Результаты хирургического лечения РП данных стадий остаются неудовлетворительными, 5 лет переживают лишь около 20% больных. В целях улучшения результатов лечения используются различные сочетания лекарственной и лучевой терапий (предоперационная ХТ, предоперационная химиолучевая терапия, самостоятельная химиолучевая терапия).
При клинической стадии IVa (Т4 или множественные метастазы в регионарных лимфатических узлах средостения) основным методом лечения является самостоятельная химиолучевая терапия. Однако вовлечение перикарда, плевры, легкого и диафрагмы не исключает возможности хирургического лечения в случае объективного ответа на предоперационную терапию.
Основными задачами лечения больных РП с отдаленными метастазами являются улучшение качества жизни путем устранения симптомов, обусловленных ростом опухоли, и увеличение продолжительности жизни. Оценка эффективности различных режимов ХТ этой категории больных затруднена в связи с отсутствием рандомизированных исследований, особенно при плоскоклеточном раке. По этой же причине сложно оценить и тот выигрыш, который дает ХТ по сравнению с симптоматической терапией.
Химиотерапия рекомендуется пациентам в удовлетворительном общем состоянии (по шкале ECOG 0-2 балла) при отсутствии выраженной (III-IV степени) дисфагии, затрудняющей адекватное питание пациента. В последнем случае на первом этапе показано восстановление проходимости пищевода (стентирование, реканализация). При дисфагии I-II степени ХТ позволяет добиться уменьшения степени ее выраженности у ряда больных уже к концу первого курса.
Наиболее эффективными препаратами при обоих гистологических вариантах являются цисплатин, фторпиримидины, таксаны.
При плоскоклеточных раках стандартным режимом ХТ остается комбинация цисплатина с инфузией 5‐фторурацила или капецитабином, частота объективных эффектов при использовании подобных режимов составляется около 35%, а продолжительность жизни не превышает 6-8 мес. Карбоплатин уступает цисплатину по непосредственной эффективности, что ограничивает его применение вне программ химиолучевой терапии.
Применение таксанов возможно в составе двухкомпонентных схем с цисплатином или трехкомпонентных комбинаций (с цисплатином и фторпиримидинами). В последнем случае ценой большей токсичности удается повысить объективный эффект до 48%, однако к удлинению продолжительности жизни это, по-видимому, не приводит.
Паллиативное лечение
Наиболее частым симптомом РП является дисфагия. Необходимость в ее устранении может возникать на всех этапах лечения. Для устранения дисфагии используются различные методы:
- эндоскопические процедуры (баллонная дилатация, электро-, аргонно-плазменная или лазерная деструкция, фотодинамическая терапия),
- лучевая терапия (дистанционная или брахитерапия),
- постановка внутрипросветных стентов.
Эндоскопические процедуры дают быстрый, но кратковременный эффект и подходят в тех случаях, когда в ближайшее время будет начато лечение с предполагаемой высокой эффективностью (хирургическое, лекарственное, лучевое).
В том случаях, когда излечение больного невозможно, оптимальными вариантами коррекции дисфагии является брахитерапия, стентирование пищевода или дистанционная лучевая терапия.
Паллиативная химиолучевая терапия не имеет явных преимуществ по сравнению с ЛТ (без ХТ) и сопряжено с большей токсичностью. По результатам исследования стентирование пищевода позволяет быстрее достичь желаемых эффектов, однако при большем сроке наблюдения в сравнении с брахитерапией частота осложнений (миграция стента, боли, перфорация, желудочно-пищеводный рефлюкс) оказалась выше, а частота полного купирования дисфагии – несколько ниже. При развитии пищеводно-бронхиальных или медиастинальных свищей постановка покрытых стентов позволяет купировать данные осложнения у 70-100% больных.
Наблюдение
Активное наблюдение показано больным для раннего выявления рецидива в пищеводе с целью выполнения хирургического вмешательства либо рецидива в средостении с целью проведения химиолучевой терапии. Объем обследования зависит от стадии болезни и предшествующего лечения:
Стадия I (после эндоскопических резекций слизистого/подслизистого слоя) и стадии II-III (после химиолучевой терапии, имеется перспектива для эзофагэктомии в случае рецидива):
- ЭГДС – каждые 3-4 мес. в течение первых двух лет, каждые 6 мес. – в течение третьего года, далее ежегодно до общей продолжительности наблюдения 5 лет.
- КТ органов грудной клетки и органов брюшной полости – каждые 6 мес. в течение первых 2 лет, далее – ежегодно до общей продолжительности наблюдения 5 лет;
Стадия I-III (после хирургического лечения):
- КТ органов грудной клетки и органов брюшной полости – каждые 6 мес. в течение первых 2 лет, далее – ежегодно до общей продолжительности 5 лет.
Другие методы обследований у остальных категорий пациентов рекомендуется выполнять при наличии клинических показаний. Выполнение ПЭТ/КТ и определение маркеров в сыворотке крови для наблюдения за пациентами не рекомендуется.
Хирургическое лечение в отделении торакоабдоминальной хирургии и онкологии РНЦХ
Лечение в отделении проводится по программам ОМС, ДМС, ВМП, а также на коммерческой основе.
Читайте, как попасть на лечение в отделение торакоабдоминальной хирургии и онкологии РНЦХ.
Для записи на консультацию позвоните по телефонам:
+7 (499) 248 13 91
+7 (903) 728 24 52
+7 (499) 248 15 55
Отправьте заявку на консультацию, заполнив форму на нашем сайте и прикрепив необходимые документы.
Источник
