Разрастание грануляционной ткани в желудке
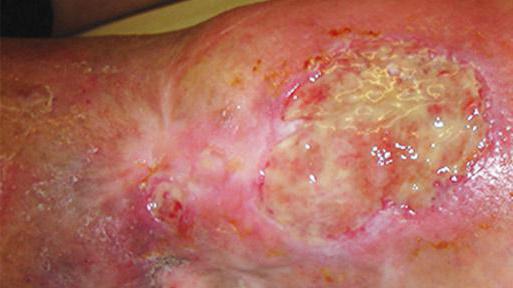
Грануляционная ткань (лат. granulum зернышко; син.: грануляция, «дикое мясо», зернистая ткань) — соединительная ткань, образующаяся при заживлении тканевых дефектов путем вторичного натяжения.

Рис. 12. Грануляционная ткань: а — слабо выраженные грануляции; — грануляционная ткань с гнойными наложениями.
Первоначально этот термин использовали только для характеристики раневых процессов, протекающих в тканях, обладающих свободной поверхностью (кожа, слизистая оболочка) и потому видимых глазом. Но он правомерен и по отношению к молодой соединительной ткани (см.), формирующейся при организации тромбов, инфарктов, воспалительных экссудатов и инкапсуляции инородных тел. Формирование Грануляционной ткани — проявление одного из трех последовательно сменяющих друг друга этапов раневого процесса — воспаления (см.), образования грануляций, рубцевания. Непосредственно за повреждением развивается травматический отек, в процессе к-рого происходит избыточное накопление жидкости в поврежденных тканях. В отечной жидкости содержится большое количество белков: альбуминов, глобулинов, фибриногена. Воспалительная реакция, сменяющая травматический отек, ведет к расплавлению мертвых тканей и очищению раны. Еще до завершения этого процесса в дне и по краям раны начинает развиваться Г. т. (цветн. рис. 12,а), постепенно заполняющая возникший дефект. Развитие Г. т. представляет собой проявление регенерации (см.). Сложное строение Г. т. подробно описано H. Н. Аничковым, К. Г. Волковой, В. Г. Гаршиным (1951). Поверхность ее покрыта некротическими массами (цветн. рис. 12,б), содержащими мелкозернистый детрит, фибрин, большое количество лейкоцитов и эритроцитов. Под этим лейкоцитарно-некротическим слоем располагается слой сосудистых петель, содержащий тонкостенные сосуды, полиморфно-ядерные лейкоциты и фибробласты. Интенсивная пролиферация эндотелиоцитов обеспечивает быстрый рост капилляров, достигающих раневой поверхности и затем, образуя петли, вновь уходящих в глубь ткани. Вершины петель с поверхности имеют вид красноватых зерен, вследствие чего молодая соединительная ткань и получила название грануляционной, зернистой. Под слоем сосудистых петель лежит слой собственно Г. т., или слой вертикальных сосудов, составляющий главную ее массу. Между вертикально расположенными сосудами этого слоя находится аморфное межуточное (основное) вещество, представляющее собой студнеобразную массу. Еще глубже лежит слой горизонтально расположенных фибробластов — созревающий слой. Этот слой, постепенно утолщаясь, играет основную роль при заживлении раны. Морфологической особенностью его является разнообразный клеточный состав: здесь находятся фибробласты, эозинофильные лейкоциты, макрофаги, тучные клетки. Глубокие участки этого слоя постепенно приобретаю* вид фиброзной ткани, составляющей дно, а часто и края раны.

Рис. 1. Электронограмма фибробласта грануляционной ткани: 1 — ядро; 2 — коллагеновые волокна; 3 — рибосомы; 4 — Эндоплазматический ретикулум; 5 — липид; 6 — митохондрии; 7 — пластинчатый комплекс (аппарат Гольджи); х 30 000.

Рис. 2. Электронно-микроскопический авторадиограф РНК фибробласта грануляционной ткани на третьи сутки после нанесения раны. Над ядром (1) и в особенности над ядрышком (2) сосредоточено большое количество зерен серебра (указаны стрелками), свидетельствующее об активном синтезе РНК в этих структурах. Многочисленные зерна серебра над цитоплазмой (3) свидетельствуют об интенсивном перемещении сюда синтезированной в ядре РНК.

Рис. 3. Электронно-микроскопический авторадиограф РНК фибробласта грануляционной ткани на 14-е сутки после нанесения раны. Сниженный, по сравнению с молодым фибробластом (рис. 2), синтез РНК в этой клетке проявляется небольшим количеством зерен (указаны стрелками) над ядром (1), ядрышком (2); 3 — цитоплазма.
На ранних этапах развития Г. т. состоит преимущественно из аморфного межуточного вещества, содержащего кислые мукополисахариды (гиалуроновая к-та, хондроитин-серная к-та, глюкозамин, галактоза-мин, гепарин); в нем рассеяны немногочисленные соединительнотканные клетки и фибробласты, гистиоциты, тучные клетки, нейтрофильные и эозинофильные лейкоциты, клетки лимфоидного ряда, или полибласты. Кислые мукополисахариды, синтезирующиеся фибробластами и тучными клетками, входят в состав коллагеновых пучков как материал, цементирующий коллагеновые фибриллы. Общая динамика развития Г. т. заключается в постепенном уменьшении количества аморфного вещества, интенсивной пролиферации клеточных элементов и сосудов, число которых в дальнейшем, по мере нарастания массы коллагеновых волокон и формирования рубца, снижается. Ведущую роль в образовании основного вещества Г. т. и особенно ее волокнистых структур играют фибробласты. Эти клетки, в обычных условиях тонкие, вытянутые, с небольшим узким ядром и цитоплазмой, бедной ультраструктурами, при активации биосинтетических процессов становятся крупными, с большим овоидным ядром и резко возросшим объемом цитоплазмы. При электронной микроскопии в таких фибробластах наблюдают увеличение числа митохондрий, гипертрофию пластинчатого комплекса (см. Гольджи комплекс) и расширение его цистерн, значительную гиперплазию шероховатого эндоплазматического ретикулума, ответственного за синтез коллагеновых белков (рис. 1). Фибробласты обладают высокой активностью гидролитических (кислые и щелочные фосфатазы) и протеолитических (аминопептидаза, катепсины) ферментов. Менее выражена в фибробластах активность окислительно-восстановительных ферментов (сукцинатдегидрогеназы, цитохромоксидазы и др.). В их цитоплазме содержится большое количество гликогена и рибонуклеопротеидов. Авторадиографическое исследование свидетельствует об интенсивном синтезе РНК в фибробластах Г. т. (рис. 2). В отношении происхождения фибробластов Г. т. существуют различные точки зрения. Одни исследователи считают более вероятным местное их происхождение из адвентициальных клеток, другие полагают, что фибробласты попадают в Г. т. гематогенным путем; существует также мнение, допускающее наличие обоих этих источников. Отмеченные у фибробластов признаки высокой биосинтетической активности в равной мере наблюдаются и в других клетках Г. т.— тучных, макрофагах, эндотелиоцитах. Тучные клетки принимают участие в образовании межуточного вещества соединительной ткани. Полагают, что, с другой стороны, они регулируют состав межклеточного вещества, поглощая избыток мукополисахаридов, откладывающихся в их цитоплазме в виде гранул. Появление и активизация тучных клеток почти исключительно в созревающем слое грануляций, в к-ром происходит постоянная убыль кислых мукополисахаридов, делают это предположение вполне обоснованным. Уменьшение массы аморфного вещества в созревающей Г. т. происходит синхронно с увеличением в ней количества волокнистых структур. Около фибробластов, лежащих вдоль вертикально расположенных сосудов, появляются нежные коллагеновые волокна. В это же время в Г. т. обнаруживают в большом количестве и аргирофильные волокна. Высокая активность фермента коллагеназы в цитоплазме фибробластов свидетельствует о том, что эти клетки, по-видимому, обеспечивают не только синтез коллагеновых волокон, но и частичный лизис их, благодаря чему достигается регуляция количества новообразований фиброзной ткани. На ранних этапах новообразования Г. т. процессы рассасывания выражены слабо. Интенсивными они становятся в период созревания грануляций, когда происходит нарастание массы коллагеновых волокон, часть которых подвергается рассасыванию. При закрытии раневого дефекта и образовании рубца стихает процесс рассасывания коллагеновых волокон. По мере созревания Г. т. количество межуточного аморфного вещества, тучных клеток, гистиоцитов, лейкоцитов и других ее клеточных элементов снижается, а количество грубеющих коллагеновых волокон увеличивается. В процессе развития рубца постепенно стихает и биосинтетическая активность фибробластов, которые превращаются в «покоящиеся» фиброциты. В этот период снижается энзиматическая активность фибробластов, в их цитоплазме уменьшается содержание гликогена и РНК (рис. 3), уменьшается количество цитоплазматических структур. В финале раневого процесса формируется рубцовая ткань, представляющая собой пучки грубых коллагеновых волокон с расположенными между ними немногочисленными фиброцитами и сосудами. Способность фиброцитов рубцовой ткани к повторному активному синтезу коллагена, т. е. превращению в фибробласты, не изучена. Позже в рубце могут появляться эластические волокна.
Развитие Грануляционной ткани характеризует процесс заживления раны путем вторичного натяжения. Если же рана невелика и ее края максимально сближены, срастание их происходит быстро, без развития значительных грануляций, и в этих случаях говорят о заживлении путем первичного натяжения. В обоих случаях клеточная реакция и динамика коллагеноза принципиально идентичны, и речь идет только о количественных различиях.
Весь цикл развития и созревания Г. т. занимает ок. 2—3 нед., однако различные этапы этого процесса могут затягиваться или протекать интенсивнее в зависимости от размеров раны, индивидуальных особенностей организма и различных условий окружающей среды. При нарушениях кровообращения, иннервации, авитаминозе С наблюдаются различные отклонения от описанного хода развития Г. т. в виде вяло текущих грануляций, появления избыточных грануляций (напр., «дикое мясо» на деснах при кариесе зубов и парадентитах, при длительном нагноении раны, хроническом остеомиелите) или быстрого и чрезмерного огрубения соединительной ткани с гиалинозом фиброзных пучков и формированием так наз. келоидных рубцов. Эти отклонения обусловлены качественными и количественными нарушениями коллагенообразования в фибробластах и окружающем их межуточном вещество.
У детей процесс развития Грануляционной ткани протекает интенсивнее, чем у взрослых. Сокращению сроков заживления ран способствуют и некоторые фармакологические препараты, напр, пентаксил, метилурацил, оротат калия.
См. также Раны, ранения.
Библиография Аничков H. Н., Волкова К. Г. и Гаршин В. Г. Морфология заживления ран, М., 1951; Давыдовский И. В. Огнестрельная рана человека, т. 1, М., 1950; Хрущов Н. Г. Проблема происхождения фибробластов в постнатальном онтогенезе млекопитающих, Онтогенез, т. 5, № 1,с. 3, 1974, библиогр.; Rae k. allio J. Enzyme histochemistry of wound healing, Progr. histochem. cyto-chem., v. 1, p. 51, 1970, bibliogr.; Repair and regeneration, ed. by J. E. Dunphy a. W. V. Winkle, p. 151, N. Y. a. o., 1969; Whitting H. The tissue mast cell and wound healing, Int. Rev. Gen. Exp. Zool., v. 4, p. 131, 1969, bibliogr.
Д. С. Саркисов.
Источник
Одной из фаз заживления поврежденной ткани является грануляция раны. Под раной подразумевается нарушение целостности кожи, мышц, костей или внутренних органов. По типу сложности раны различаются в зависимости от степени повреждения. На этом основании доктор делает прогноз, назначает лечение. Огромную роль в процессе выздоровления играет грануляционная ткань, которая образуется при заживлении ран. Каким образом она образуется, что собой представляет? Разберемся более подробно.
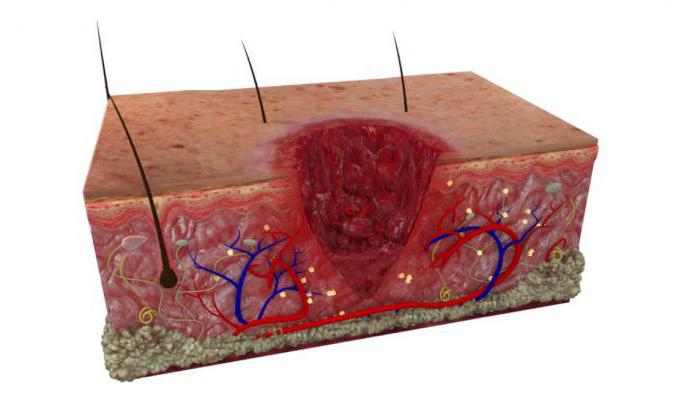
Как выглядит грануляционная ткань
Грануляционной тканью называют молодую соединительную ткань. Она развивается во время заживления раны, язвы, при инкапсуляции инородного тела.
Здоровая, нормальная грануляционная ткань имеет розово-красный цвет, зернистую структуру и плотную консистенцию. Отделяется из нее в небольших количествах мутный серовато-белый гнойный экссудат.
Возникает такая ткань на границах между мертвой и живой, после ранения на 3-4-е сутки. Состоит грануляционная ткань из множества гранул, которые тесно прижаты друг к другу. В их состав входят: амфорные вещества, петлевидные сосудистые капилляры, гистиоциты, фибробласты, полибласты, лимфоциты, многоядерные блуждающие клетки, аргирофильные волокна и сегментоядерные лейкоциты, коллагеновые волокна.
Образование грануляционной ткани
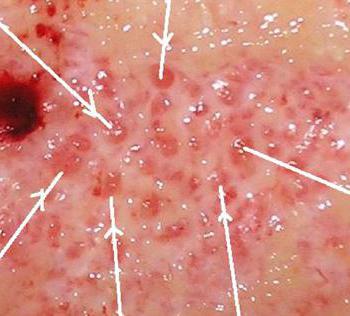
Уже через двое суток на свободных от кровяных сгустков и некротизированной ткани участках можно заметить розово-красные узелки – величиной с просяное зерно гранулы. На третий день количество гранул значительно возрастает и уже на 4-5-е сутки поверхность раны покрывает молодая грануляционная ткань. Хорошо этот процесс заметен на резаной ране.
Здоровые крепкие грануляции розовато-красного цвета, они не кровоточат, имеют равномерный зернистый вид, очень плотную консистенцию, выделяют небольшое количество гнойного мутного экссудата. В нем содержится большое количество погибших клеточных элементов местной ткани, гнойные тельца, примеси эритроцитов, сегментоядерные лейкоциты, та или иная микрофлора с продуктами собственной жизнедеятельности. В данный экссудат происходит эмиграция клеток ретикулоэндотелиальной системы, белых кровяных телец, сюда же врастают сосудистые капилляры и фибробласты.
По причине того что в зияющей ране новообразованным капиллярам невозможно соединиться с капиллярами противоположной стороны раны, они, загибаясь, образуют петли. Каждая из таких петель является каркасом для вышеуказанных клеток. Из них формируется каждая новая гранула. Ежедневно рана заполняется все новыми гранулами, так происходит полное стягивание всей полости.
Слои
Слои грануляционной ткани разделяются:
- на поверхностный лейкоцитарно-некротический;
- слой самой грануляционной ткани;
- фиброзный глубокий слой.

Со временем рост капилляров и клеток идет на убыль, возрастает количество волокон. Грануляционная ткань начинает превращаться сначала в волокнистую, а далее в рубцовую.
Главная роль грануляционной ткани – барьерные функции, она препятствует попаданию в рану микробов, токсинов, продуктов распада. Она угнетает жизнедеятельность микробов, разжижает токсины, связывает их, помогает отторгать некротизированные ткани. Грануляции заполняют полость дефекта, раны, создается тканевый рубец.
Заживление раны
Грануляции всегда образуются на границах между живой и омертвевшей тканью. Быстрее они формируются, когда в поврежденной ткани хорошее кровообращение. Бывают случаи, когда грануляции образуются в разные сроки, неравномерно развиваются. Зависит это от количества в ткани мертвых клеток и сроков их отторжения. Чем быстрее происходит грануляция, тем скорее заживление ран. После очищения раны от мертвых тканей и воспалительного экссудата становится хорошо заметен грануляционный слой. Иногда в медицинской практике требуется удаление грануляционной ткани, чаще всего это применяется в стоматологии при гингивотомии (разрезе десны).
Если отсутствуют какие-либо причины, препятствующие заживлению, грануляционной тканью заполняется вся полость раны. Когда грануляции достигают уровня кожи, они начинают уменьшаться в объемах, становятся немного бледнее, затем покрываются кожным эпителием, он разрастается от периферии к центру повреждения.
Заживление первичным и вторичным натяжением
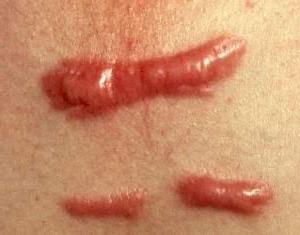
Заживление ран может происходить первичным или вторичным натяжением, в зависимости от их характера.
Для первичного натяжения характерно сокращение краев раны благодаря соединительнотканной организации грануляции. Она прочно соединяет края раны. После первичного натяжения рубец остается почти незаметным, гладким. Такое натяжение способно затянуть края раны небольшой, если противоположные стороны находятся на расстоянии не более одного сантиметра.
Вторичное натяжение характерно для заживления ран больших, где имеется множество нежизнеспособных тканей. Значительные дефекты или все гнойные раны проходят путь заживления вторичным натяжением. Отличаясь от первичного вида, вторичное натяжение имеет полость, которую и заполняет грануляционная ткань. Рубец после вторичного натяжения имеет бледно-красный цвет, немного выдается за поверхность кожи. По мере того как в нем постепенно загустевают сосуды, развивается волокнистая и рубцовая ткань, происходит ороговение кожного эпителия, рубец начинает бледнеть, становится плотнее и уже. Иногда развивается гипертрофия рубца – это когда образуется избыточное количество рубцовой ткани.
Заживление под струпом
Третий вид заживления раны самый простой – рана заживает под струпом. Это характерно для незначительных ран, повреждений кожного покрова (ссадины, царапины, потертости, ожоги 1-й, 2-й степени). Струп (корка) на поверхности раны образуется из крови, которая там свернулась, лимфы. Роль струпа – защитный барьер, который ограждает рану от проникновения инфекций, под этим щитом происходит регенерация кожи. Если процесс идет нормально, не попала никакая инфекция, после заживления корка отходит без следа. На коже не остается никаких признаков, что когда-то здесь присутствовала рана.
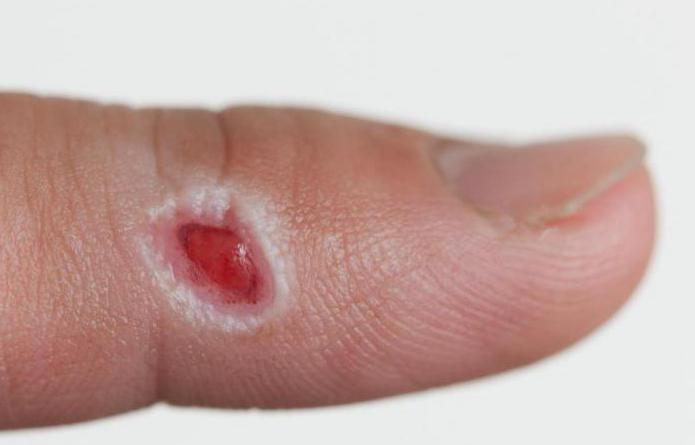
Патологии грануляции
Если раневой процесс нарушен, могут образовываться патологические грануляции. Возможен недостаточный или избыточный рост грануляционной ткани, распад грануляций, преждевременный склероз. Во всех этих случаях, а также если грануляционная ткань кровоточит, потребуется специальное лечение.
Развитие грануляций и процессы эпителизации угасают, если есть такие неблагоприятные факторы, как ухудшение кровоснабжения, декомпенсация каких-либо систем и органов, оксигенации, повторный гнойный процесс. В этих случаях развиваются патологии грануляции.
Клиника при этом такова: отсутствует сокращение раны, меняется внешний вид грануляционной ткани. Рана выглядит бледной, тусклой, теряет тургор, становится синюшной, покрывается налетом гноя и фибрина.
Патологическими считаются и бугристые грануляции, когда они выступают за края раны, – гипергрануляции (гипертрофические). Нависая над краями раны, они препятствуют процессу эпителизации. В этих случаях их прижигают концентрированными растворами перманганата калия или нитрата серебра. Рану продолжают лечить, стимулируя эпителизацию.
Значение грануляционной ткани
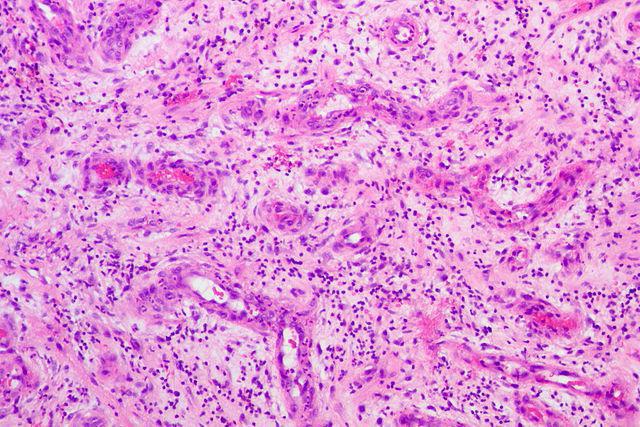
Итак, подводя итоги, выделим основные роли, которые играет грануляционная ткань:
- Замещение дефектов ран. Грануляции – пластический материал, который заполняет рану.
- Защита раны от попадания инородных тел, проникновения организмов, токсинов. Достигается это благодаря большому количеству лейкоцитов, макрофагов, а также плотной структуре.
- Отторжение и секвестрация некротических тканей. Способствует процессу наличие макрофагов, лейкоцитов, а также протеолитические ферменты, которые выделяют клеточные элементы.
- При нормальном ходе заживления одновременно с грануляцией начинается эпителизация. Грануляционная ткань трансформируется в грубоволокнистую ткань, далее образуется рубец.
Источник
Патологические грануляции
Обязательным элементом заживления ран является образование грануляционной ткани. Её состояние определяет характер раневого процесса и скорость заживления раны. Но не всегда в ране образуется нормальная грануляционная ткань. При воздействии ряда неблагоприятных факторов развитие грануляций может носить патологический характер. Нарушения кровообращения, декомпенсация функции различных органов и систем, приводящих к различным нарушениям обмена, вторичное инфицирование и повторное развитие гнойного процесса могут приводить к угасанию образования грануляционной ткани. В таких случаях грануляции становятся бледными, иногда серыми, тусклыми, рыхлыми, покрываются налетом фибрина и гноя. В таких случаях рана длительно не заживает.
В некоторых случаях может наблюдаться образование гипертрофических грануляций. Такие грануляции бугристые, выступают за пределы раны, нависают над её краями, препятствуя эпителизации. С целью борьбы с избыточным образованием грануляционной ткани приходится или иссекать их, или применять прижигающие препараты (нитрат серебра, перманганат калия).
Рубцы
Результатом раневого процесса является заживление раны с образованием рубца. Рубец остается на всю жизнь, и он может не только доставлять косметические неудобства пациенту, но и быть субстратом для развития патологического процесса. Эти обстоятельства диктуют необходимость в процессе лечения ран предвидеть какой рубец сформируется и предпринимать действия направленные на формирование наиболее косметически и функционально выгодных рубцов.
Вид, характер и свойства рубца зависят в первую очередь от вида заживления раны. При заживлении первичным натяжением рубец обычно линейный, тонкий, подвижный, ровный, находится на одном уровне со всей поверхности кожи. По своей консистенции он сходен с окружающими тканями.
В случае заживления вторичным натяжением рубец обычно имеет неправильную форму. По консистенции он плотный, малоподвижный, по цвету отличается от окружающей кожи. Поверхность рубца располагается ниже поверхности кожи, поэтому он втянут.
Как видно, рубцы, образующиеся при вторичном заживлении, хуже, чем при первичном заживлении. Поэтому следует стремиться к заживлению ран первичным заживлением.
В процессе образования рубца в результате влияния ряда факторов могут формироваться гипертрофические и келоидные рубцы.
Нормальный рубец состоит из нормальной соединительной ткани. Если в процессе рубцевания имеется избыточный синтез коллагена, то рубец будет состоять из плотной фиброзной ткани. Такие рубцы грубые, уродливые, возвышаются над поверхностью кожи, отличаются по цвету от окружающей ткани. Они могут длительное время доставлять беспокойство больным, т. к. болезненны, зудят.
Наихудшим вариантом завершения процесса рубцевания является образование келоидного рубца.
Обычный гипертрофический рубец соответствует размерам раны и не распространяется на окружающие ткани. Отличительной чертой келоидного рубца является то, что он внедряется в окружающие нормальные ткани.
Келоидные рубцы могут возникать после любой, даже незначительной травмы, поверхностного ожога. Келоид по морфологической структуре представляет собой незрелую соединительную ткань с большим количеством атипичных гигантских фибробластов. Патогенез формирования келоида до настоящего времени не совсем ясен. Определенную роль играют генетические нарушения, обуславливающие нарушения синтеза коллагена и механизмы аутоагрессии на собственную незрелую соединительную ткань.
Келоидный рубец начинает развиваться через 1-3 месяца после окончания эпителизации раны, и рост его может продолжаться до 2 лет. С течением времени он не уменьшается и не размягчается.
Лечение келоидных рубцов трудная задача. В начальных стадиях применяют электрофорез с лидазой. Сформировавший келоидный рубец иссекают с наложением косметического внутрикожного шва. В послеоперационном периоде в течение всего процесса заживления воздействуют на рану ферметами, стероидными гормонами, проводят лучевую терапию. Эффективных способов профилактики образования келоидных рубцов до настоящего времени не найдено.
Осложнения рубцов
Возможно развитие следующих осложнений рубцов:
1. Рубцовые контрактуры;
2. Изъязвления рубца;
3. Папилломатоз рубца;
4. Опухолевое перерождение рубцовой ткани (малигнизация).
Вышеуказанные осложнения наиболее часто возникают в рубцах, сформировавшихся при заживлении ран вторичным натяжением.
Рубцовая контрактура-это деформация рубцами окружающих тканей, приводящая к нарушению функций вовлеченных структур. В случае расположения таких рубцов в области суставов отмечается уменьшений объема движений. При рубцах на лице, шее, промежности может отмечаться нарушение функции расположенных там анатомических структур. Учитывая, что рубцовая контрактура, развивается при обширных ранах, методом профилактики является выполнение кожной пластики.
Изъязвления появляются на гипертрофических и келоидных рубцах, особенно если они постоянно подвергаются постоянной травматизации.
Папилломатоз рубцов и малигнизация также развиваются на гипертрофических рубцах, подвергающихся длительное время травматизации.
ЛЕКЦИЯ 18
Источник
