Полипы желудка и пищевода лечение
Полип пищевода — это доброкачественное эзофагеальное новообразование на ножке или широком основании с экзофитным типом роста, происходящее из эпителиальной оболочки органа. Зачастую протекает бессимптомно. Может проявляться дисфагией, болями за грудиной и в эпигастрии, диспепсией, затруднением дыхания. Диагностируется с помощью эзофагогастродуоденоскопии, контрастной рентгенографии пищевода и гистологического исследования биоптата. Лечится хирургическими методами, для удаления полипа проводится эндоскопическая электроэксцизия, электрокоагуляция, лазерная коагуляция, лигирование или клипирование.
Общие сведения
Полипы пищевода — сравнительно редкий вариант доброкачественных эзофагеальных неоплазий, выявляемый у 0,5-3% пациентов. Заболеванию более подвержены мужчины старше 40 лет. Новообразования могут формироваться в любом участке органа, но чаще локализуются в местах физиологических сужений на передней эзофагеальной стенке. До 80-85% полипов располагается в нижней трети пищевода. Неоплазии бывают единичными и множественными. В области гастроэзофагеального перехода в 57-58% случаев выявляются полипы на широком основании, в нижней и средней трети — опухоли на ножке, склонные к эрозированию.

Полип пищевода
Причины и факторы риска
Возникновение полипа пищевода обычно связано с частым воздействием различных повреждающих факторов на слизистую оболочку органа. Определенную этиологическую роль играет наследственная склонность пациента к гиперрегенерации, сопровождающаяся множественным полипозом. По мнению специалистов в сфере современной гастроэнтерологии и онкологии, основными предпосылками к формированию эзофагеальных полипов являются:
- Воспалительные процессы. В 80-85% случаев полипы возникают на фоне гастроэзофагеальной рефлюксной болезни, аллергического, дисметаболического и других хронических эзофагитов, провоцируются повреждением слизистой под действием инфекционных агентов, медиаторов воспаления. Полипоз нижнего отдела пищевода часто ассоциируется с рефлюкс-гастритом.
- Травматические повреждения. Толчком к неогенезу могут стать механические травмы эпителия, действие термических и химических факторов, в том числе острые химические ожоги сильнодействующими реагентами (кислотами, щелочами). В редких случаях полипы образуются после линейных разрывов эзофагеальной слизистой у больных, перенесших синдром Меллори-Вейса.
- Пищевые привычки. Потенцирующим фактором полипообразования является постоянное раздражение эпителиального слоя острой, горячей, кислой и грубой пищей, которое стимулирует процессы гиперрегенерации слизистой и облегчает развитие воспаления. В группу риска также входят больные, злоупотребляющие крепкими алкогольными напитками.
Факторы риска
Возникновению полипов способствует длительное пребывание в неблагоприятных экологических условиях, частые стрессовые ситуации, курение. Некоторые авторы рассматривают в качестве причины полипообразования в месте кардиоэзофагеального перехода нарушение эмбриогенеза слизистой, приводящее к дистопии эмбриональных тканей, из которых формируются эпителиальные неоплазии.
Причины
Патогенез полипов пищевода основан на гиперрегенерации эзофагеальных эпителиоцитов под действием повреждающих факторов. Воспалительные процессы, травмы, раздражение пищей и химически активными веществами стимулирует избыточную пролиферацию эпителия и нарушает его дифференцировку. В результате на некоторых участках слизистой формируются очаги гиперплазии, из которых образуются полипы. В зависимости от типа клеток, участвующих в неопластическом процессе, полипозные новообразования бывают гиперпластическими (с типичной клеточной структурой) и аденоматозными (с дисплазией железистых эпителиоцитов).
Симптомы полипов пищевода
Заболевание длительное время протекает бессимптомно, что объясняется маленькими размерами и медленным ростом новообразования. Первыми признаками полипов пищевода являются дискомфорт и незначительные боли при проглатывании твердой пищи. По мере прогрессирования болезни и увеличения размеров неоплазии возникает тошнота и рвота после еды, отмечается отрыжка, периодическое или постоянное ощущение умеренной боли за грудиной, нарушения дыхания, связанные со сдавливанием воздухоносных путей крупным полипом. При расположении полипов на ножке в нижней части пищевода зачастую выявляются резкие боли в эпигастральной области, вызванные ущемлением опухоли при смыкании кардиального сфинктера. Общее состояние пациентов обычно не нарушено.
Осложнения
При длительном течении заболевания происходит постоянная мацерация полипов частичкам пищи, что со временем приводит к эрозиям и изъязвлениям. Иногда открывается массивное кровотечение из эзофагеальных сосудов, представляющее опасность для жизни больного. Неинтенсивные повторные кровопотери вызывают железодефицитную гипорегенераторную анемию с характерной бледностью кожных покровов и слизистых, головокружением, мельканием «мушек» перед глазами, общей слабостью. Наиболее опасное осложнение полипов пищевода — малигнизация с формированием эзофагеального рака или аденокарциномы: озлокачествление гиперпластических новообразований происходит в 0,25-7,1% случаев, аденоматозных — в 18-75%. У пациентов также может возникать кахексия, которая обусловлена невозможностью полноценного энтерального питания на поздних стадиях заболевания.
Диагностика
Новообразование зачастую выявляется случайно при эндоскопическом диагностическом обследовании по поводу другой патологии ЖКТ. В начальном периоде болезни, характеризующемся бессимптомным течением, постановка диагноза затруднена. О возможном наличии у пациента полипов пищевода свидетельствуют длительно существующие жалобы на перемежающую дисфагию и загрудинные боли неустановленной этиологии. Диагностический поиск направлен на комплексное лабораторно-инструментальное обследование верхних отделов пищеварительного тракта. Наиболее информативными являются:
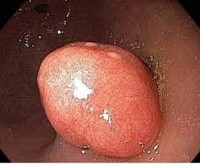
- Эзофагогастродуоденоскопия. Исследование при помощи гибкого эндоскопа — «золотой стандарт» в диагностике полипов. При осмотре обнаруживается розовое или ярко-красное округлое образование на ножке, которое частично закрывает просвет органа. Прикосновение инструмента вызывает кровоточивость. Во время ЭФГДС производится забор материала для морфологического анализа.
- Рентгенография пищевода. Для выявления полипов выполняется серия рентгеновских снимков после перорального введения контрастного вещества. Если размер опухоли превышает 10 мм, на рентгенограмме визуализируется дефект наполнения округлой формы с четкими контурами. Полипозное новообразование менее 1 см в диаметре выглядят как утолщенная складка слизистой оболочки.
- Гистология биоптата пищевода. Изучение образцов ткани, взятых при эндоскопии, требуется для оценки морфологического типа неоплазии, дифференциальной диагностики между доброкачественными и злокачественными новообразованиями. Для полипов характерно сохранение гистологической структуры всех слоев слизистой, отсутствие атипичных клеток с патологическими митозами.
Изменения в клиническом анализе крови (снижение количества гемоглобина и эритроцитов) появляются при развитии железодефицитной анемии вследствие изъязвления полипов и кровотечения. В биохимическом анализе крови может обнаруживаться гипоальбуминемия, обусловленная недостаточным питанием. Дополнительно выполняется реакция Грегерсена (на скрытую кровь в кале) для исключения кровотечений из нижних отделов ЖКТ. При недостаточной информативности других методов назначается КТ или МРТ.
Дифференциальная диагностика проводится с функциональными заболеваниями пищевода (ахалазией, кардиоспазмом, эзофагоспазмом), дивертикулами, злокачественными новообразованиями, воспалительной патологией (рефлюкс-эзофагитом, туберкулезным эзофагитом). При загрудинных болях необходимо исключить ишемическую болезнь сердца, бронхолегочную патологию. В рамках дифдиагностики, помимо осмотра гастроэнтеролога, пациенту рекомендована консультация кардиолога, пульмонолога.
Лечение полипов пищевода
При наличии одного или нескольких небольших гиперпластических полипов пищевода, случайно обнаруженных при эндоскопическом исследовании верхних отделов ЖКТ и не проявляющихся клинически, возможно динамическое наблюдение за пациентом с лечением основного заболевания (ГЭРБ, эзофагита, рефлюкс-гастрита), коррекцией диеты и проведением контрольных эзофагоскопий каждые 6-12 месяцев. Консервативных методов терапии заболевания не существует. Обнаружение гистологически подтвержденных аденоматозных новообразований, их интенсивный рост (более чем в 1,5 раза за год), размеры свыше 5 мм, повышенная кровоточивость, сочетание с воспалением и эрозией, возникновение выраженной клинической симптоматики служат показаниями для оперативного удаления полипов. Пациентам с эзофагеальным полипозом проводятся:
- Эндоскопическая полипэктомия. Наиболее часто применяется электроэксцизия и электрокоагуляция опухолевидного образования под контролем эндоскопа. Реже выполняется лазерная фотокоагуляция. Иногда ложе полипа (оставшийся участок ножки или широкое основание, оставшиеся после отсечения неоплазии) коагулируются химическим путем.
- Лигирование и клипирование полипов. Вмешательства также проводятся эндоскопическим методом и предполагают накладывание лигатуры (клипсы) после захвата новообразования и окружающей его слизистой. Преимуществом методики является меньшая инвазивность, позволяющая снизить риск возникновения послеоперационного кровотечения или перфорации.
Прогноз и профилактика
Исход болезни зависит от своевременности диагностики и морфологического варианта образования. При гиперпластическом полипе пищевода, который отличается доброкачественным течением, прогноз благоприятный. При аденоматозных неоплазиях существует высокий риск злокачественной трансформации, что при отказе от оперативного лечения значительно ухудшает прогноз для пациента. Меры специфической профилактики патологии не разработаны. Для предупреждения полипозных разрастаний необходимо проводить раннее выявление и лечение воспалительных заболеваний пищевода, избегать употребления грубой, плохо пережеванной пищи, ограничить прием алкоголя.
Источник
Полип желудка – это ненормальное разрастание ткани, исходящей из слизистой оболочки желудка. Они встречаются довольно-таки редко и обычно не вызывают клинических симптомов. Полипы желудка диагностируются, когда доктор проводит исследование по какой-либо другой причине.
Дальнейшее отношение к выявленному во время видеоэзофагогастродуоденоскопии (ВГДС) полипу зависит от его гистологической верификации, этиологии (причины возникновения), естественной истории (развитие в динамике). После оценки полученных данных решается вопрос о необходимости лечения в данном клиническом случае или о проведении динамического наблюдения.
Классификация полипов желудка
Наиболее рациональным является классифицирование полипов по клиническим, морфологическим и гистологическим признакам. Чаще всего полипы имеют бессимптомное течение. Однако, осложненный вариант может проявляться кровотечением (признаки анемии, кровь в стуле), непроходимостью (тошнота, рвота), гастритоподобным течением (боли в верхних отделах живота) и малигнизацией (снижение массы тела и др. симптомы онкологического заболевания).
По морфологическим критериям полипы разделяют на солитарные (одиночные) и множественные, мелкие и крупные, мягкие и плотные. Учитывая, что видеогастроскопия является «золотым» стандартом в диагностике данной патологии, во всем мире признанной является Парижская классификация эпителиальных новообразований, согласно которой выделяют выступающие (0-Ip – на узкой ножке, 0-Isp – на зауженном основании, 0-Is – сидячие) и поверхностные (0-IIa – приподнятые, 0-IIb – поверхностные плоские, 0-IIc – слегка углубленные, смешанные варианты).
Ключевым моментом при выполнении эндоскопического исследования является не только правильная интерпретация найденного образования, но и возможность забора материала с последующим гистологическим подтверждением, что главным образом влияет на дальнейшую тактику лечения. В связи с этим представлены четыре группы полипов с их подробными характеристиками.
Полипы фундальных желез
Наиболее частый тип полипов, выявляемых при ЭГДС. По данным крупных современных исследований, фундальные полипы желудка диагностируются приблизительно в 6% пациентов, которым проводится ЭГДС. Это, в свою очередь, cоставляет около 74% всех полипов желудка, подтвержденных гистологической оценкой. Эндоскопически фундальные полипы желудка обычно множественные, небольшие (менее 10 мм), с гладкой поверхностью, блестящие и макроскопически «сидячие» (0-Is по Парижской классификации 2002-2005 гг.)
При хромоскопии и узкоспектральной эндоскопии (NBI) поверхность представлена рисунком по типу «пчелиных сот» с густой сосудистой архитектоникой. Изначально фундальные полипы связывали с гамартомами (образованиями, представляющими тканевую аномалию развития), однако, в большом числе исследований подтверждено, что механизмы, подавляющие секрецию соляной кислоты ингибиторами протонной помпы (ИПП), могут также участвовать в патогенезе развития фундальных полипов желудка.
Гистологически фундальные полипы представлены дилятированными (расширенными) кислотопродуцирующими железами, покрытыми плоскими париетальными и слизистыми клетками без признаков дисплазии. Выявление характерных полипов желудка у пациентов, принимающих ИПП, с большой долей вероятности диагностируют как полипы фундальных желез. При первичном осмотре один или более представленных полипов после взятия биопсии подвергают морфологической оценке для подтверждения диагноза. Большие полипы (более 10 мм), эрозированные, расположенные нетипично, например, в антральном отделе желудка, должны быть подвергнуты более агрессивной тактике ведения – эндоскопической полипэктомии.
Гиперпластические полипы
Это воспалительная пролиферация фовеолярных клеток желудка (муцин – продуцирующих эпителиальных клеток). Гиперпластические полипы желудка связывают с атрофией слизистой, вызванной инфицированием H.pylori или аутоиммунными гастритами. Однако, в последнее время встречается все больше случаев выявления таких полипов на фоне нормальной или реактивной слизистой, не связанной с сопутствующей инфекцией. Гиперпластические полипы в равной степени встречаются у мужчин и женщин на 6 -7 декадах жизни. Наиболее частая локализация – это антральный отдел желудка.
Эндоскопически они обычно гладкие, куполообразные (0-Is, 0-Isp тип), размерами от 5 до 15 мм в диаметре, хотя могут быть намного больше. Большие полипы становятся дольчатыми, расположенными на ножке (0-Ip тип), поверхность эпителия полипа нередко эрозирована, что может являться причиной хронической кровопотери и железодефицитной анемии. Редко поступают пациенты с признаками высокой непроходимости, вследствие обтурации или пролабирования полипа через привратник. Гиперпластические полипы возникают как гиперпролиферативный ответ на повреждение слизистой (эрозии, язвы). Длительное химическое воздействие соляной кислоты и наличие инфекции H.pylori могут быть первоначальной ступенью в их развитии.
Гистологическая характеристика включает удлиненные, искаженные, разветвленные, дилятированные фовеолярные железы с богато васкуляризованной стромой на фоне хронического воспаления. Показано, что в 1 – 20 % полипов могут скрываться фокусы диспластических изменений. В целом, распространенность очага карциномы составляет менее 2 % и, как правило, в полипах размерами более 20 мм. В связи с потенциальным риском развития рака желудка, все гиперпластические полипы более 10 мм в диаметре следует полностью удалять. Резекция полиповидных образований всегда должна быть дополнена взятием образцов интактной слизистой, которые содержат информацию о распространенности и тяжести воспалительных и атрофических изменений в окружающей слизистой оболочке (по морфологической классификации OLGA). В результате – определяется стратификация риска развития рака желудка.
По современным представлениям, необходимо выполнить эрадикацию H.pylori с последующей оценкой между 3 и 6 месяцами после терапии для подтверждения успешного лечения. Во многих случаях оставленные маленькие гиперпластические полипы могут регрессировать или исчезнуть вовсе. Пациенты с III и IV стадиями по классификации OLGA (умеренная диффузная или тяжелая атрофия слизистой, наряду с распространенной кишечной метаплазией) должны проходить последующее эндоскопическое наблюдение не реже 1 раза в год, так как риски развития рака желудка в данном случае повышаются более чем в 6 раз.
Аденома желудка
Наиболее частый желудочный неопластический полип – это эпителиальное диспластическое разрастание ткани, часто называемое аденомой, по современной номенклатуре ВОЗ-интраэпителиальная неоплазия. В западном, индустриально развитом мире, H.pylori – связанные аденомы желудка становятся редки, насчитывая менее 1%, хотя встречаемость рака желудка и аденом в регионах Восточной Азии остается высокой, около четверти всех полипов. Как и гиперпластические полипы, аденомы желудка встречаются с одинаковой частотой у мужчин и у женщин, на 6-7 декадах жизни.
Эндоскопически они представлены солитарным одиночным образованием дольчатой формы с бархатистой поверхностью. Хотя они могут быть найдены в любом отделе, наиболее часто локализуются в антральном отделе желудка.
Аденомы желудка состоят из диспластических эпителиальных клеток, которые часто появляются на фоне атрофии и интестинальной метаплазии слизистой, естественным образом связанными с инфекцией H.pylori. Аденомы могут быть рассмотрены как часть последовательной цепочки от дисплазии к раку желудка. Имеется прямо пропорциональная связь – чем больше аденоматозный полип, тем выше вероятность наличия в нем фокуса аденокарциномы. Учитывая тот факт, что аденома, возникающая на фоне хронического атрофического гастрита, является предшественником аденокарциномы, должно быть рекомендовано полное удаление (резекция) всех аденоматозных полипов с оценкой тяжести воспалительных и атрофических изменений слизистой желудка. Важно то, что аденома – это неопластическое образование, и поэтому всех пациентов с выявленными аденомами необходимо внести под эндоскопическое наблюдение, несмотря на стадию атрофии слизистой. Эрадикационная терапия H.pylori с последующим подтверждением эффективности лечения также должна быть оценена в ходе гистологического исследования.
Нейроэндокринные опухоли (НЭО)
Карциноиды – нейроэндокринные опухоли, исходящие из энтерохромаффинноподобных (ЭХ) клеток. НЭО составляют менее 2% полиповидных образований, желудка и подразделяются на три основных типа.
- НЭО I типа составляют 70-80% всех нейроэндокринных опухолей. Они ассоциированы с гипергастринемией вследствие аутоиммунного атрофического гастрита, более того, они встречаются у пожилых пациентов, чаще женщин с атрофическим гастритом на фоне пернициозной анемии. Эти образования обнаруживаются случайно, они маленькие (менее 10 мм), множественные, морфологически состоящие из эндокринных клеток с низким пролиферативным индексом (не склонны к озлокачествлению).
- НЭО II типа связаны с гипергастринемией вследствие гастрин-секретирующей опухоли. Она является одной из составляющих таких синдромов как МЭН-1 и Золлингера-Эллисона. Этот тип опухоли достаточно редок, составляет лишь 5 – 8 % всех НЭО. В этом случае опухоль менее 1 см, без характерных инфильтративных изменений, окружающая слизистая оболочка либо нормальная, либо умеренно воспалена, но без атрофических явлений. НЭО желудка I и II типов могут быть удалены эндоскопически, с последующим подавлением секреции гастрина медикаментозно.
- НЭО III типа встречаются спорадично. Составляют около 20% всех НЭО и обычно обнаруживаются при появлении клинической симптоматики (боль в эпигастрии) или при эрозировании слизистой (проявляется кровотечением), или при обнаружении метастазов (наличие карциноидного синдрома – гиперемия кожи, диарея, бронхоспазм, патология клапанной системы сердца). Данный тип опухоли имеет склонность к достижению размеров более 1,5 см, с полиморфными изменениями слизистой (эрозирование, зоны некроза, инфильтрации слизистой). Пролиферативный индекс (KI-67, индекс митотической активности) составляет более 20%, что говорит о злокачественном течении заболевания, требующего хирургической тактики лечения.
Лечение полипов желудка
Как говорилось ранее, все аденоматозные и крупные полипы более 10 мм должны быть подвергнуты удалению. Каким же образом выполняется эндоскопическая полипэктомия или резекция слизистой?
После четкого определения границ образования, под его основание в подслизистый слой выполняется инъекция физиологического раствора, окрашенного красителем «индигокарминовый синий» с целью предотвращения перфорации и четкой визуализации сосудистых структур. Затем эндоскопическая петля позиционируется на неизмененной слизистой вокруг образования и постепенно затягивается. Далее выполняется электрокоагуляция с использованием электрохирургического ножа/блока. Пострезекционный дефект с белым струпом без «плюс ткани» говорит о радикальности и надежности оперативного вмешательства, тем самым исключая возможные осложнения. Этапы операции представлены на рисунках (в нашей Клинике используется нож – ERBE VIO 300D).
Крупные экзофитные (выступающие) полипы на широком основании или плоские образования, которые невозможно удалить эндопетлей, подвергаются технически более сложному варианту эндоскопического удаления – диссекции в подслизистом слое. Данный вид операции направлен на радикальное удаление образования единым блоком: после создания «гидростатической подушки» выполняется циркулярный разрез вокруг образования специальными инструментами, после чего рассекаются соединительнотканные сплетения подслизистого слоя с полной ликвидацией патологического очага.
Послеоперационное наблюдение
Первые сутки после полипэктомии рекомендуется щадящий режим активности и питания. Как упоминалось ранее, на месте полипа остается пострезекционный дефект слизистой оболочки, в связи с чем назначается противоязвенная диета – стол №1 по Певзнеру. Суть его заключается в ограничении продуктов, стимулирующих секрецию в желудке, длительно задерживающихся и трудно перевариваемых блюд (острая, жирная, жареная пища). Такая диета и ограничение физических нагрузок соблюдаются в течение месяца. Также необходимо помнить об отказе от приема антикоагулянтов в течение 3 дней как перед, так и после операции, в целях предотвращения ранних и отсроченных кровотечений.
По современным представлениям, наиболее рациональным является наблюдение за пациентами после проведенной полипэктомии через 1 год. При этом оценивается состояние слизистой оболочки на предмет появления новых образований или рецидива на месте ранее выполненной операции. Если же после резекции образований гистологический ответ подтверждает наличие дисплазии высокой степени или же раннего рака, то контрольная гастроскопия должна проводиться в интервале: 1,5 мес.- 3 мес.- 6 мес. – 1 год и в последующем каждый год.
Профилактика полипов желудка
Целью профилактики является выявление образований желудка на ранних этапах развития. Рекомендуется выполнение эндоскопического исследования лицам старше 45 лет в качестве скрининга даже при отсутствии клинической симптоматики, так как заболевание проявляет себя лишь на поздней стадии, когда уже требуется хирургическое лечение. Следуя принципам онкологической настороженности, пациентам с отягощенным наследственным анамнезом, то есть при наличии онкологических заболеваний со стороны ЖКТ у ближайших родственников, требуется незамедлительный профилактический осмотр желудка и толстой кишки.
Как получить услугу в Клинике
В нашей Клинике проводятся все виды эндоскопических исследований на высококачественном оборудовании как под местной анестезией, так и под наркозом. Все выявленные патологические образования подвергаются гистологической верификации. Также проводится забор материала на наличие инфекции H.pylori и для определения стадии и степени выраженности воспалительных и атрофических изменений слизистой оболочки желудка (класс.OLGA), что свидетельствует, как говорилось ранее, о риске развития онкологического процесса.
Что касается оперативного эндоскопического лечения, то в клинике возможно его выполнение в амбулаторных и стационарных условиях. Решение принимает лечащий врач, опираясь на размеры патологических очагов, их количество, результаты гистологии и сопутствующую патологию.
Источник
