Клинический случай рак желудка
По материалам:A multidisciplinary approach to an unusual medical case of locally advanced gastric cancer: a case report
Nicola Carlomagno, Fabrizio Schonauer, Vincenzo Tammaro, Annalena Di Martino, Carmen Criscitiello, Michele L. Santangelo
Journal of Medical Case Reports 2015, 9:13
81‑летняя женщина поступила в терапевтическое отделение с жалобами на общую слабость, потерю веса, рвоту и боли в животе. В анамнезе: гипертоническая болезнь и холецистэктомия по поводу острого холецистита. При осмотре обнаружена припухлость на передней брюшной стенке, высказано предположение о послеоперационной грыже. Однако при эндоскопическом исследовании выявлена опухоль антрального отдела желудка. В следующие несколько дней над описанной припухлостью образовалась сначала небольшая кожная язва, а затем сформировался свищ. Пациентка была переведена в хирургическое отделение.
Для справки
Пан-цитокератин (общий цитокератин, цитокератин АЕ1/АЕ3) — смесь моноклональных антител к различным цитокератинам, белкам цитоскелета эпителиальных клеток. Используется для дифференциальной диагностики рака и неэпителиальных опухолей.
Хромогранин А содержится в гранулах большинства нейроэндокринных клеток. Специфичный маркер нейроэндокринных опухолей разного происхождения.
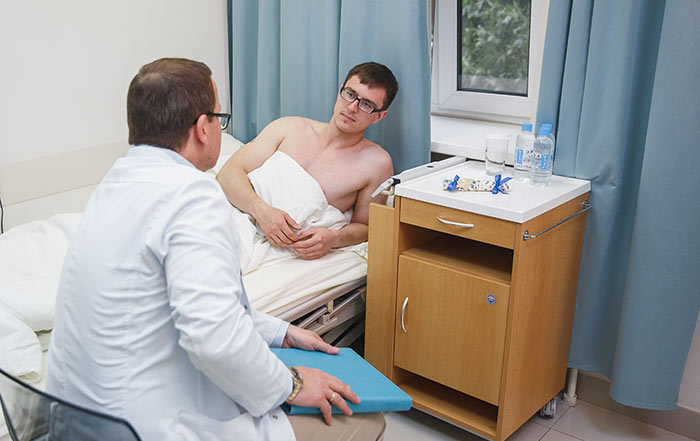
При лабораторном исследовании выявлены гипопротеинемия 46 г/л, гипоальбуминемия 20 г/л и анемия (гемоглобин 83 г/л). При выполнении компьютерной томографии (КТ) описано массивное образование 10×14×15 см в области антрума с центральным некрозом и кровоизлияниями, со слабой васкуляризацией, без четкой границы с левой долей печени (рис. 1). Опухолевая масса врастала в поперечную ободочную кишку и прямую мышцу живота, занимала значительную часть верхнего этажа брюшной полости и формировала наружный свищ. При КТ-исследовании не обнаружено метастазов.
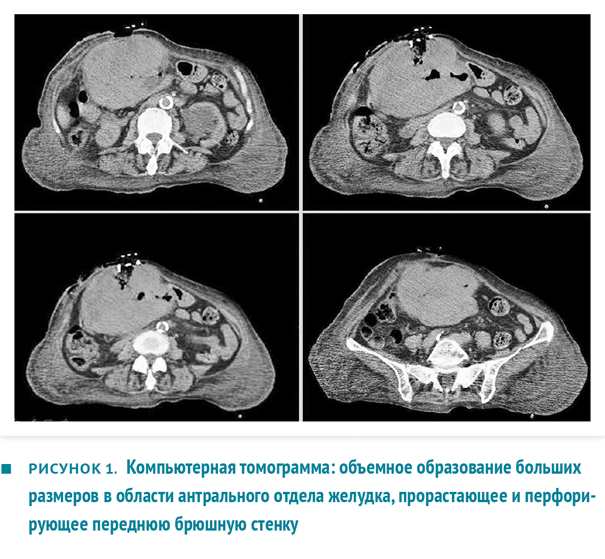
Проведено хирургическое лечение. Вокруг неопластического поражения выполнен эллиптический разрез в пределах 2 см здоровых тканей (рис. 2). Боковые края расширены линейными разрезами.
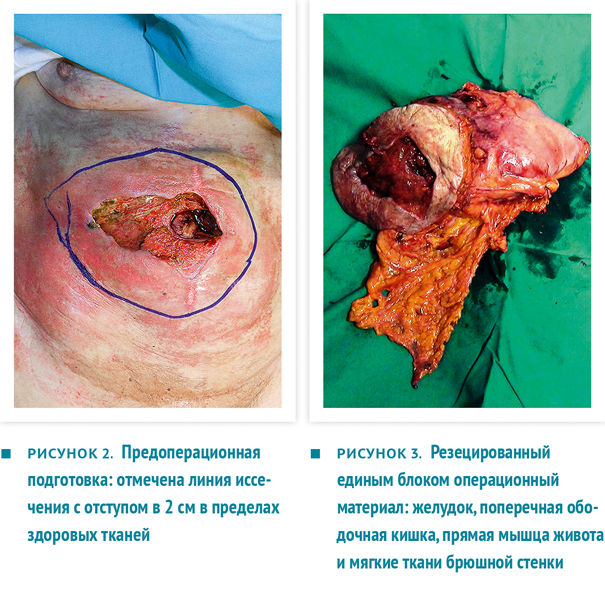
Единым блоком резецированы участок передней брюшной стенки, часть желудка и часть ободочной кишки (рис. 3), проведена систематическая лимфодиссекция, после чего наложен аппаратный гастроеюноанастомоз и ручной тонко-толстокишечный анастомоз. Установлены 2 внутрибрюшных дренажа (рис. 4).
Дефект передней брюшной стенки протезирован сетчатым трансплантатом, рана закрыта методом реверсивной абдоминопластики (рис. 5). Внутрибрюшное давление в ходе оперативного вмешательства и в послеоперационном периоде было
ниже 10 мм. рт. ст.
Для справки
CD56 — молекула клеточной адгезии, в норме экспрессируется на поверхности натуральных киллеров, нейронов, клеток глии, скелетных мышц. Определяется на клетках многих солидных и гематологических опухолей.
Виментин — белок цитоскелета клеток мезодермального происхождения, в частности соединительной ткани. Обнаруживают при фиброзных опухолях, саркомах, мезотелиоме.
Синаптофизин участвует в формировании синаптических пузырьков в нервных клетках. Маркер нейроэндокринных опухолей.
Белок S-100 — семейство кальций-связывающих белков, повышение концентрации наблюдается при прогрессии меланомы.
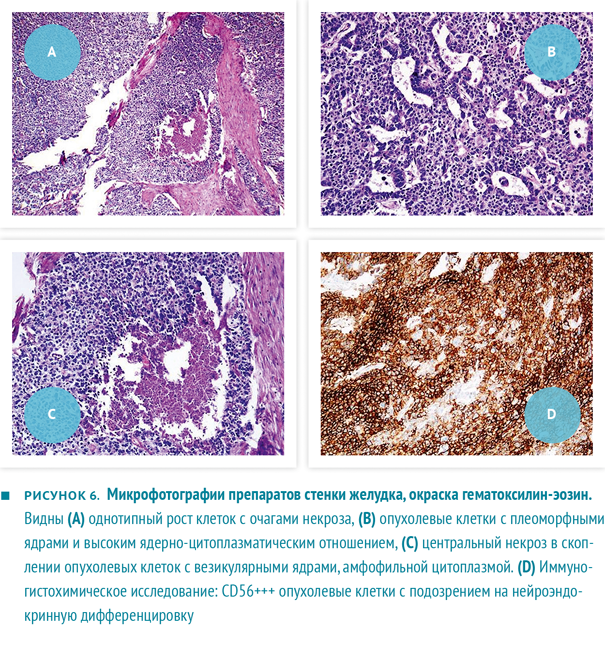
По данным гистологического исследования, удаленная опухоль соответствовала малодифференцированной аденокарциноме с чертами нейроэндокринной дифференцировки с прорастанием до слизистой оболочки поперечной ободочной кишки и мягких тканей до кожи (рис. 6а‑с). При иммуногистохимическом исследовании выявлено позитивное окрашивание к пан-цитокератину, хромогранину и CD56 (рис. 6d), негативное — к виментину, синаптофизину и S-100.
Состояние пациентки в раннем послеоперационном периоде было удовлетворительным. По поводу анемии легкой степени проведены гемотрансфузии в первые 3 дня. Активная перистальтика отмечена с 3‑го дня. С 6-го дня, после контрастного рентгенологического исследования верхних отделов ЖКТ, пациентка начала самостоятельно принимать пищу.
К сожалению, с 10‑го дня у пациентки на фоне пневмонии развился тяжелый респираторный дистресс-синдром. Несмотря на проводимую антибактериальную терапию и перевод в отделение интенсивной терапии, она умерла на 20‑й день после операции.
Обсуждение
Несмотря на то что рак желудка часто обнаруживают только на поздних стадиях [1, 2], прорастание опухолью брюшной стенки с ее деструкцией и формированием наружного желудочного свища встречается редко. Обычно поражение опухолевыми клетками ограничивается серозными оболочками и прилежащими тканями смежных органов [3]. В литературе описаны единичные случаи серьезного поражения кишечника при раке желудка и манифестации болезни с кишечной непроходимости [4–7], прямокишечного кровотечения, запоров и тенезмов [8]. Еще более редки случаи доминирования симптомов массивного прорастания брюшной стенки. Описан 62‑летний пациент с диффузной инвазией опухолевых клеток в переднюю брюшную стенку при раке желудка, однако без ее полного разрушения [9].
Ранее опубликованы случаи гастроинтестинальных стромальных опухолей желудка, достигавших гигантских размеров и отличавшихся быстрым ростом по сравнению со «средними» аденокарциномами [10, 11], но в данном случае описан ранее не представленный тип этой опухоли — нейроэндокринный.
Публикация клинического случая и сопутствующих иллюстраций осуществлялись с одобрения родственников пациентки. Копия подписанного информированного согласия находится у главного редактора журнала «Journal of medical case reports».
В запущенных случаях рака желудка возможности терапии обычно ограничены неоадъювантной химиотерапией с гастростомией или еюностомией. В описанном случае подобная тактика была неприменима из‑за обширного дефекта брюшной стенки и вовлечения поперечной ободочной кишки. Было принято решение о резекции всех пораженных органов единым блоком.
При онкологических операциях во избежание контаминации опухолевыми клетками распространено широкое иссечение больших участков мягких тканей. Устранение кожного дефекта после оперативных вмешательств возможно пластикой на питающей ножке местными и отдаленными тканями, либо с переносом свободного кожного лоскута [1]. Для реконструкции дефекта верхней части передней брюшной стенки могут быть использованы кожно-мышечные лоскуты на основе прямой мышцы живота или широчайшей мышцы спины. При значительном поражении местных тканей может потребоваться свободная кожная пластика. Ее преимущество — лучший косметический эффект, а недостатки — более длительное время операции, возможность отторжения трансплантированного лоскута и большие повреждения донорского участка.
Альтернативой перечисленным методам может быть использованная в описанном случае реверсивная абдоминопластика [12]. Кожу нижнего края операционной раны вместе с поверхностной фасцией отделяют от мышечного футляра. Разрез продолжают до лобковой области, полученный лоскут подтягивают кверху для закрытия дефекта брюшной стенки. Реверсивная абдоминопластика чаще используется в пластической хирургии для коррекции формы живота после значительной потери веса [13, 14] и редко — для реконструктивных операций после резекции опухоли [15–17]. Она может быть использована в комбинации с другими типами лоскутов, а также для покрытия сетчатого эндопротеза.
Стоит отметить особо, что смерть пациентки наступила не из‑за хирургических осложнений. Внутрипузырное измерение внутрибрюшного давления рутинно проводили на всех этапах терапии, наиболее угрожаемых по развитию внутрибрюшной гипертензии и абдоминального компартмент-синдрома. Оперативное вмешательство проведено усилиями хирурга-онколога и пластического хирурга с применением адекватной техники. Авторы статьи убеждены в пользе и важности индивидуального подхода и нестандартных решений в сложных случаях хирургического вмешательства при онкологических заболеваниях.
Список источников
- Santangelo M, et al. Extended total gastrectomy: indications in the 3rd millennium. Minerva Chir. 2001;56 (1):1–6.
- Tammaro V, et al. Prognostic value of splenectomy and lymph-node dissection during gastric cancer resection. Chir Ital. 2006;58 (2):163–70.
- Feczko PJ, et al. Metastatic disease involving the gastrointestinal tract. Radiol Clin North Am. 1993;31:1359–73.
- Tomikashi K, et al. Gastric cancer metastatic to the colon. Gastrointest Endosc. 2002;55:561.
- Kumagai K, et al. Octreotide acetate successfully treated a bowel obstruction caused by peritoneally disseminated gastric cancer, thereby enabling the subsequent use of oral S-1 chemotherapy. Int J Clin Oncol. 2009;14:372–5.
- Fukuda Y, et al. A case of advanced gastric cancer with direct invasion of the transverse colon responding to paclitaxel/5′-DFUR combined therapy. Gan To Kagaku Ryoho. 2005;32:1945–8.
- Yu X, Zhang J. Gastric cancer with large bowel obstruction as the first presentation: a case report. Oncol Lett. 2013;6:1377–9.
- Alegre R, et al. Gastric cancer: an unusual presentation. Acta Gastroenterol Latinoam. 2003;33 (1):29–32.
- Waguri N, et al. A case of gastric cancer with abdominal wall invasion treated by weekly low-dose paclitaxel therapy. Gan To Kagaku Ryoho. 2006;33 (8):1151–4.
- Aomatsu N, et al. A case of emergency resection of a giant gastrointestinal stromal tumor of the stomach associated with hemorrhagic shock. Gan To Kagaku Ryoho. 2013;40 (12):2185–7.
- Okada K, et al. A case of gastrointestinal stromal tumor of the stomach with rapid growth in a short term. Gan To Kagaku Ryoho. 2008;35 (12):2080–2.
- Halbesma GJ, van der Lei B. The reverse abdominoplasty: a report of seven cases and a review of English-language literature. Ann Plast Surg. 2008;61:133–7.
- Akbas H, et al. The combined use of classic and reverse abdominoplasty on the same patient. Plast Reconstr Surg. 2002;109:2595–6.
- Hurwitz DJ. Single-staged total body lift after massive weight loss. Ann Plast Surg. 2004;52:435–41.
- Pantelides NM, et al. Reverse abdominoplasty: a practical option for oncological trunk reconstruction. Eplasty. 2013;13: e2.
- Bury TF, et al. Closure of massive chest wall defects after full-thickness chest wall resection. Ann Plast Surg. 1995;34:409–14.
- Dagregorio G, Darsonval V. Aesthetic surgery techniques after excision of dermatofibrosarcoma protuberans: a case report. Br J Plast Surg. 2005;58:556–60.
Источник
Рак желудка – злокачественная опухоль, которая развивается из клеток слизистой оболочки желудка. По распространенности он занимает пятое место среди всех видов рака. Как правило, болеют люди старше 40 лет. Основной метод лечения – хирургический, удаление всего желудка или его пораженной части.
Причины рака желудка
Точные причины рака желудка неизвестны. В слизистой оболочке органа возникают мутации ДНК, и получаются «неправильные» клетки, которые могут приобрести способность к неконтролируемому росту. Почему это происходит — не совсем понятно. Зато хорошо изучены факторы риска — условия, которые повышают риск рака желудка.
Наследственность и рак желудка
Некоторые люди носят в себе «бомбу замедленного действия», спрятанную в генах. Иногда даже не одну. Это подтверждается некоторыми фактами:
- Если у близкого родственника (родители, братья, сестры, дети) человека диагностирован рак желудка, его риски повышены примерно на 20%.
- Мужчины болеют чаще, чем женщины. Сложно сказать, с чем конкретно это связано, но можно предположить, что замешана разница между мужскими и женскими генами.
- Японцы, которые мигрировали в США, болеют раком желудка реже соотечественников, но чаще, чем «коренные» американцы. Это говорит о том, что дело не только в характере питания, но и в наследственности. Главный подозреваемый — ген под названием RNF43.
- Карцинома — самый распространенный тип рака желудка — чаще встречается у людей с группой крови A (II), которую они, конечно же, получили вместе с генами.
- Риски повышены при некоторых наследственных заболеваниях: злокачественной анемии (в 3-6 раз), гипогаммаглобулинемии, неполипозном раке толстой кишки.
- Заболеваемость раком желудка повышается после 70 лет: считается, что это происходит из-за того, что с возрастом в клетках тела накапливаются нежелательные мутации.
Рак желудка и характер питания
Роль питания в возникновении злокачественных опухолей желудка изучена хорошо. Риски повышает большое количество соли, крахмала, нитратов, некоторых углеводов. Чаще болеют люди, которые едят много соленых, копченых, маринованных продуктов, мало овощей и фруктов.

Рак желудка и вредные привычки
Курение повышает риск рака желудка примерно вдвое. Ученые в Великобритании считают, что примерно каждый пятый случай связан именно с курением. Когда человек вдыхает табачный дым, часть его попадает в желудок, и содержащиеся в нем вредные вещества повреждают клетки слизистой оболочки. Риски тем выше, чем больше стаж курильщика и ежедневное количество сигарет. Алкоголь тоже в списке подозреваемых, но прямых доказательств пока нет.
Хеликобактер пилори (H. Pylori) и рак желудка
H. Pylori — бактерия, которая способна вызывать язвенную болезнь и хронический атрофический гастрит. В настоящее время она считается важным фактором развития рака желудка. При хеликобактерной инфекции вероятность возникновения злокачественной опухоли в желудке повышается в 4 раза. В половине удаленных опухолей обнаруживают этого возбудителя.
Другие факторы риска
- Язвенная болезнь. Данные исследований по этому поводу противоречивы. Если язва находится в теле желудка, риск рака повышается почти в 2 раза. При язве нижнего отдела риски, видимо, не повышаются.
- Аденоматозные полипы слизистой оболочки.
- Семейный аденоматозный полипоз – заболевание, вызванное мутацией в гене APC и приводящее к возникновению множества полипов в желудке, кишечнике. При этом незначительно повышается риск рака.
- Перенесенные на желудке операции повышают риск рака в 2,5 раза. Это происходит из-за того, что желудок производит меньше соляной кислоты, и в нем активнее размножаются бактерии, продуцирующие нитриты, происходит обратный заброс желчи из тонкой кишки. Обычно злокачественные опухоли возникают спустя 10-15 лет после хирургического вмешательства.
- Социальное и материальное положение: риск увеличивается при низком уровне доходов, проживании в перенаселенной квартире, без удобств, в неблагоприятном районе.
- Другие онкологические заболевания: рак пищевода, простаты, мочевого пузыря, молочных желез, яичников, яичек.
- Болезнь Менетрие (гипертрофическая гастропатия) характеризуется разрастанием слизистой оболочки желудка, появлением в ней складок и снижением продукции соляной кислоты. Патология встречается редко, поэтому неизвестно, как часто она приводит к раку желудка.
- В группе повышенного риска работники угольной, металлургической и резиновой промышленности.
- Иммунодефицит повышает вероятность развития рака, лимфомы желудка.
Классификация рака желудка: каким он бывает?
Злокачественные опухоли желудка, согласно Международной гистологической классификации ВОЗ, делят на 11 типов, в зависимости от того, из каких клеток они происходят. Преобладает рак из железистых клеток, которые выстилают слизистую оболочку и вырабатывают слизь — аденокарцинома. Он составляет 90-95% всех случаев. Также встречаются опухоли из иммунных (лимфома), гормонпродуцирующих (карциноид) клеток, из нервной ткани.
Одна из старейших классификаций делит злокачественные опухоли желудка на 3 типа:
- Кишечный. Как следует из названия, в окружении опухоли имеется кишечная метаплазия, то есть слизистая оболочка желудка становится похожа на слизистую кишечника. Этот тип рака чаще встречается у пожилых людей, отличается более благоприятным прогнозом. Это типично «японский» тип рака.
- Диффузный. Опухолевые клетки расползаются по стенке желудка, они окружены нормальной слизистой оболочкой.
- Смешанный.
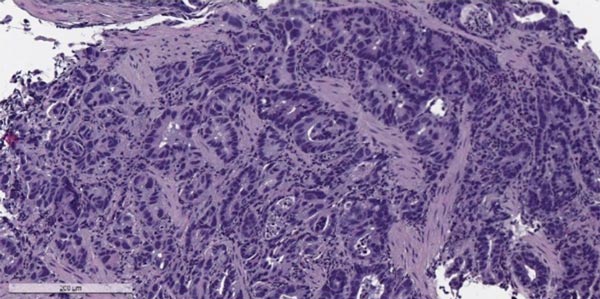
Аденокарцинома желудка
Стадии рака желудка
Рак желудка делят на ранний (начальный) и распространенный. При раннем опухоль не прорастает глубже слизистой оболочки и подслизистой основы. Такие опухоли проще удалить (в том числе эндоскопическим путем), при них лучше прогноз. Также используют классификацию TNM, которая учитывает размеры и прорастание в разные ткани первичной опухоли (T), метастазы в регионарных (близлежащих) лимфатических узлах (N), отдаленные метастазы (M).
Классификация в зависимости от состояния первичной опухоли (T):
- Tx – первичную опухоль невозможно оценить;
- T0 – первичная опухоль не обнаруживается;
- T1 – тяжелая дисплазия клеток слизистой оболочки, опухоль находится в поверхностном слое слизистой оболочки (“рак на месте”);
- T2 – опухоль проросла в мышечный слой стенки органа;
- T3 – рак достиг серозной (наружной) оболочки желудка, но не пророс в нее;
- T4 – опухоль проросла в серозную оболочку (T4a), в соседние структуры (T4b).
Классификация в зависимости от наличия поражения в регионарных лимфатических узлах:
- Nx – невозможно оценить метастазы в лимфатических узлах;
- N0 – метастазы в регионарных лимфоузлах не обнаружены;
- N1 – поражены 1-2 лимфоузла;
- N2 – опухолевые клетки распространились в 3-6 лимфоузлов;
- N3 – метастазы в 7-15 (N3a) или в 16 и более (N3b) лимфоузлах.
Классификация в зависимости от наличия отдаленных метастазов:
- M0 – отдаленные метастазы не обнаружены;
- M1 – обнаружены отдаленные метастазы.
Аденокарциному делят на 4 стадии:
- I стадия (T1M0N0 – стадия Ia; T1N1M0, T2N0M0 – стадия Ib). Опухоль находится в пределах слизистой оболочки и подслизистой основы, не прорастает вглубь стенки желудка. Иногда раковые клетки обнаруживают в близлежащих лимфатических узлах.
- II стадия (T1N2M0, T2N1M0, T3N0M0 – стадия IIa; T1N3aM0, T2N2M0, T3N1M0, T4aN0M0 – стадия IIb). Опухоль прорастает в мышечный слой стенки желудка и распространяется в лимфатические узлы.
- III стадия (T2N3aN0, T3N2M0, T4aN1M0, T4aN2M0 – стадия IIIa; T1N3bM0, T2N3bM0, T3N3aM0, T4aN3aM0, T4bN1M0 – стадия IIIb; T3N3bM0, T4aN3bM0, T4bN3aM0 – стадия IIIc). Рак пророс через всю стенку желудка и, возможно, распространился на соседние органы, успел сильнее поразить близлежащие лимфатические узлы.
- IV стадия (любые T и N, M1). Есть отдаленные метастазы.
Метастазы рака желудка
Раковые клетки могут отрываться от материнской опухоли и мигрировать в другие части тела различными путями:
- С током лимфы они могут попасть в лимфатические узлы брюшной полости, а из них — в лимфоузлы надключичной области — метастаз Вирхова. Метастаз в лимфоузлы, окружающие прямую кишку, называют метастазом Шницлера.
- С током крови раковые клетки чаще всего распространяются в печень, реже — в легкие.
- Также раковые клетки могут рассеиваться по брюшной полости. Если они оседают на яичниках, образуется метастаз Крукенберга, в пупке — метастаз сестры Марии Джозеф.Редко при раке желудка обнаруживают метастазы в головном мозге, костях.
Симптомы: как проявляется рак желудка?
На ранних стадиях рак желудка либо не имеет симптомов вообще, либо маскируется под другие заболевания: гастрит, обострение язвенной болезни. Ухудшение аппетита и боли под ложечкой редко заставляют людей сразу же подозревать онкозаболевание и бежать в больницу. Обычно ограничиваются диетой и приемом разрекламированных таблеток «от желудка». Если человек уже страдает язвенной болезнью, он может воспринять первые признаки рака желудка как очередное обострение язвы. И уже позже, когда диагностировано онкологическое заболевание, больной вспоминает, что проявления были «не такими, как всегда».

Существует так называемый «синдром малых признаков» — его сформулировал один из основоположников советской онкологии, Александр Иванович Савицкий. Если беспокоят похожие симптомы — это повод сходить к врачу и провериться:
- Необъяснимая слабость и повышенная утомляемость.
- Плохой аппетит.
- Снижение работоспособности.
- Потеря веса.
- «Желудочный дискомфорт»: неприятные ощущения, из-за которых даже любимая еда больше не радует.
В дальнейшем нарастают более яркие, «кричащие» признаки. Они зависят от того, в какой части органа находится опухоль:
- Дисфагия. Возникает, если новообразование сдавливает место перехода желудка в пищевод. Сначала становится сложно глотать твердую пищу, затем и жидкую.
- Рвота недавно съеденной пищей. Характерна для опухолей в нижней части желудка, в месте перехода в двенадцатиперстную кишку.
- Стойкая изжога.
- Постоянные боли в области желудка, которые отдают в спину. Они не проходят ни днем, ни ночью.
- Потеря веса.
- Увеличение живота. Возникает из-за асцита — скопления жидкости в брюшной полости.
- Под ложечкой можно почувствовать и нащупать жесткое выпирающее образование. Это — опухоль, которая срослась с передней брюшной стенкой.
Со временем в опухоли начинаются процессы изъязвления и распада, развивается желудочное кровотечение. Проявляется оно в виде черного дегтеобразного стула, рвоты, которая выглядит как «кофейная гуща» или содержит примеси алой крови. Если человек теряет много крови, он становится бледным, возникает слабость, головокружение. У некоторых людей рак диагностируется, когда их приводят в клинику в таком состоянии на машине «Скорой помощи».
Как вовремя диагностировать заболевание? Что такое скрининг, и почему он важен?
Статистика говорит о том, что в 75% случаев рак желудка диагностируют уже на распространенной стадии, когда опухоль успевает прорасти в соседние ткани, дать метастазы. Лечить таких больных сложно, прогноз, как правило, неблагоприятный. Обычно выраженные симптомы говорят о том, что рак уже успел распространиться по организму.
Как проверить желудок на рак: на ранних стадиях помогает скрининг — регулярные обследования людей, которые не испытывают никаких симптомов. В качестве скринингового исследования применяют гастроскопию — эндоскопическое исследование, во время которого в желудок вводят гибкую трубку с миниатюрной видеокамерой и лампочкой на конце. Насколько эффективна гастроскопия? Лучше всего это демонстрирует японский опыт. Распространенность рака желудка в Японии очень высока, а смертность от него одна из самых низких в мире. Достичь этого удалось благодаря внедрению массового скрининга.
В Европейской онкологической клинике существуют специальные скрининговые программы, которые помогают вовремя диагностировать разные онкологические заболевания. Посетите врача, узнайте о своих рисках и получите индивидуальные рекомендации по поводу скрининга.
Какие методы диагностики может назначить врач?
Помимо гастроскопии, программа диагностики рака желудка может включать:
- Рентгенографию, перед которой пациенту дают выпить контрастный раствор. При этом контуры желудка хорошо видны на снимках.
- Компьютерную томографию, позитронно-эмиссионную томографию.
- Диагностическую лапароскопию. Это операция, во время которой в живот пациента через отверстия вводят лапароскоп с миниатюрной видеокамерой и специальные инструменты. Процедура помогает оценить, как далеко за пределы желудка успел распространиться процесс.
- Биопсию. Врач получает образец подозрительной ткани и отправляет в лабораторию для изучения под микроскопом. Этот метод диагностики помогает максимально точно диагностировать онкологическое заболевание и установить тип рака. Биопсию можно провести во время гастроскопии, хирургического вмешательства.
Современные принципы лечения рака желудка
Основной метод лечения рака желудка — хирургический. Объем операции зависит от того, на какой стадии обнаружена опухоль. Если она не успела распространиться вглубь стенки органа, проводят эндоскопическую резекцию — удаление пораженного участка при помощи инструмента, введенного через рот, как во время гастроскопии.
При субтотальной гастрэктомии удаляют часть органа, пораженную опухолевым процессом. На более поздних стадиях орган приходится удалять целиком вместе с окружающими тканями. При этом пищевод соединяют с тонкой кишкой. Если лимфатические узлы в брюшной полости поражены метастазами, их также нужно удалить.
В запущенных случаях, когда излечение невозможно, проводят паллиативную операцию. Хирург удаляет пораженную часть желудка, чтобы облегчить состояние пациента.
Лучевая терапия при раке желудка бывает:
- неоадъювантной — проводится перед операцией, чтобы уменьшить размеры опухоли и облегчить её удаление;
- адъювантной — чтобы уничтожить раковые клетки, которые остались в организме после операции.
Наиболее распространенные побочные эффекты лучевой терапии при облучении области живота: тошнота, нарушение пищеварения, диарея.
Химиотерапия также бывает адъювантной и неоадъювантной. Часто её сочетают с лучевой терапией. Химиолучевая терапия может стать основным методом лечения при метастатическом раке на поздних стадиях, когда прогноз неблагоприятный, но есть возможность облегчить симптомы и продлить жизнь больного.
В некоторых случаях эффективны таргетные препараты: трастузумаб, рамуцирумаб, иматиниб, сунитиниб, регорафениб. Но они подходят лишь в тех случаях, когда опухолевые клетки обладают определенными молекулярно-генетическими свойствами.
Какой прогноз при раке желудка?
Прогноз при раке желудка зависит от стадии опухоли, на которой был установлен диагноз и начато лечение. Шансы на стойкую ремиссию наиболее высоки, если опухоль не проросла за пределы слизистой оболочки и подслизистой основы. При метастазах прогноз, как правило, неблагоприятен.
В онкологии существует такой показатель, как пятилетняя выживаемость. Он показывает, какой процент больных остаются живы в течение 5-ти лет. Срок достаточно большой, в определенном смысле его можно приравнять к выздоровлению. Пятилетняя выживаемость при разных стадиях рака желудка составляет:
- I стадия — 57-71%;
- II стадия — 33-46%;
- III стадия — 9-20%;
- IV стадия — 4%.
Некоторые цифры и факты:
- Эксперты Всемирной организации здравоохранения (ВОЗ) утверждают, что ежегодно от рака желудка во всем мире погибают 754 000 людей.
- В XXI веке распространенность заболевания снижается, но в разных странах неодинаково. Так, на одного больного из Великобритании приходится двое из России и трое из Японии.
- По распространенности среди прочих онкозаболеваний рак желудка занимает пятое место, но среди причин смерти — третье.
- Одна из лидирующих стран по распространенности рака – Япония, во многом за счет характера питания.
В Европейской онкологической клинике применяются наиболее современные методы лечения рака желудка и других онкологических заболеваний. Даже если прогноз неблагоприятен, это не означает, что больному ничем нельзя помочь. Наши врачи знают, как облегчить симптомы, обеспечить приемлемое качество жизни, продлить жизнь
Цены на лечение рака желудка на 1-4 стадиях в Европейской онкологической клинике
- Консультация онколога — 5100 руб.
- Лечение рака желудка — от 60000 руб.
- Проведение внутриплевральной химиотерапии (инфузия, без стоимости лекарственных препаратов) — 21900 руб.
- Проведение иммунотерапии (без стоимости лекарственных препаратов) — 17200 руб.
Источник
