Активация пепсина в желудке
Под действием гастринов в главных клетках желудочных желёз стимулируются синтез и секреция пепсиногена – неактивной формы пепсина. Пепсиноген – белок, состоящий из одной полипептидной цепи с молекулярной массой 40 кД. Под действием НСl он превращается в активный пепсин (молекулярная масса 32,7 кД) с оптимумом рН 1,0-2,5. В процессе активации в результате частичного протеолиза от N-конца молекулы пепсиногена отщепляются 42 аминокислотных остатка, которые содержат почти все положительно заряженные аминокислоты, имеющиеся в пепсиногене. Таким образом, в активном пепсине преобладающими оказываются отрицательно заряженные аминокислоты, которые участвуют в конформационных перестройках молекулы и формировании активного центра. Образовавшиеся под действием НСl активные молекулы пепсина быстро активируют остальные молекулы пепсиногена (аутокатализ). Пепсин в первую очередь гидролизует пептидные связи в белках, образованные ароматическими аминокислотами (фенилаланин, триптофан, тирозин) и несколько медленнее – образованные лейцином и дикарбоновыми аминокислотами. Пепсин – эндопептидаза, поэтому в результате его действия в желудке образуются более короткие пептиды, но не свободные аминокислоты.
11
. Образование и роль соляной кислоты
Основная пищеварительная функция желудка заключается в том, что в нём начинается переваривание белка. Существенную роль в этом процессе играет соляная кислота. Белки, поступающие в желудок, стимулируют выделение гистамина и группы белковых гормонов – гастринов (см. раздел 11), которые, в свою очередь, вызывают секрецию НСI и профермента – пепсиногена. НСI образуется в обкладочных клетках желудочных желёз в ходе реакций, представленных на рис. 9-2.
Источником Н+ является Н2СО3, которая образуется в обкладочных клетках желудка из СО2, диффундирующего из крови, и Н2О под действием фермента карбоангидразы (карбонатдегидра-тазы):
Н2О + СО2 → Н2СО3 → НСО3- + H+
Диссоциация Н2СО3 приводит к образованию бикарбоната, который с участием специальных белков выделяется в плазму в обмен на С1-, и ионов Н+, которые поступают в просвет желудка путём активного транспорта, катализируемого мембранной Н+/К+-АТФ-азой. При этом концентрация протонов в просвете желудка увеличивается в 106 раз. Ионы С1- поступают в просвет желудка через хлоридный канал.
Концентрация НСl в желудочном соке может достигать 0,16 М, за счёт чего значение рН снижается до 1,0-2,0. Приём белковой пищи часто сопровождается выделением щелочной мочи за счёт секреции большого количества бикарбоната в процессе образования НСl.
Под действием НСl происходит денатурация белков пищи, не подвергшихся термической обработке, что увеличивает доступность пептидных связей для протеаз. НСl обладает бактерицидным действием и препятствует попаданию патогенных бактерий в кишечник. Кроме того, соляная кислота активирует пепсиноген и создаёт оптимум рН для действия пепсина.
Механизм активации пепсина
Под действием гастринов в главных клетках желудочных желёз стимулируются синтез и секреция пепсиногена – неактивной формы пепсина. Пепсиноген – белок, состоящий из одной полипептидной цепи с молекулярной массой 40 кД. Под действием НСl он превращается в активный пепсин (молекулярная масса 32,7 кД) с оптимумом рН 1,0-2,5. В процессе активации в результате частичного протеолиза от N-конца молекулы пепсиногена отщепляются 42 аминокислотных остатка, которые содержат почти все положительно заряженные аминокислоты, имеющиеся в пепсиногене. Таким образом, в активном пепсине преобладающими оказываются отрицательно заряженные аминокислоты, которые участвуют в конформационных перестройках молекулы и формировании активного центра. Образовавшиеся под действием НСl активные молекулы пепсина быстро активируют остальные молекулы пепсиногена (аутокатализ). Пепсин в первую очередь гидролизует пептидные связи в белках, образованные ароматическими аминокислотами (фенилаланин, триптофан, тирозин) и несколько медленнее – образованные лейцином и дикарбоновыми аминокислотами. Пепсин – эндопептидаза, поэтому в результате его действия в желудке образуются более короткие пептиды, но не свободные аминокислоты.
12.с.402
13.с.402
Соседние файлы в предмете Биохимия
- #
- #
- #
- #
- #
- #
- #
- #
27.01.202069.31 Кб1BKh_28-45.odt
- #
- #
- #
Источник
А. Переваривание белков в желудке
Желудочный сок – продукт нескольких типов клеток. Обкладочные (париетальные) клетки стенок желудка образуют соляную кислоту, главные клетки секретируют пепсиноген. Добавочные и другие клетки эпителия желудка выделяют муцинсодержащую слизь. Париетальные клетки секретируют в полость желудка также гликопротеин, который называют “внутренним фактором” (фактором Касла). Этот белок связывает “внешний фактор” – витамин В12, предотвращает его разрушение и способствует всасыванию.
1. Образование и роль соляной кислоты
Основная пищеварительная функция желудка заключается в том, что в нём начинается переваривание белка. Существенную роль в этом процессе играет соляная кислота. Белки, поступающие в желудок, стимулируют выделение гистамина и группы белковых гормонов -гастринов , которые, в свою очередь, вызывают секрецию НСI и профермента – пепсиногена. НСI образуется в обкладочных клетках желудочных желёз Источником Н+ является Н2СО3, которая образуется в обкладочных клетках желудка из СО2, диффундирующего из крови, и Н2О под действием фермента карбоангидразы (карбонатдегидратазы):
Н2О + СО2 → Н2СО3 → НСО3- + H+
Диссоциация Н2СО3 приводит к образованию бикарбоната, который с участием специальных белков выделяется в плазму в обмен на С1-, и ионов Н+, которые поступают в просвет желудка путём активного транспорта, катализируемого мембранной Н+/К+-АТФ-азой. При этом концентрация протонов в просвете желудка увеличивается в 106 раз. Ионы С1- поступают в просвет желудка через хлоридный канал.
Концентрация НСl в желудочном соке может достигать 0,16 М, за счёт чего значение рН снижается до 1,0-2,0. Приём белковой пищи часто сопровождается выделением щелочной мочи за счёт секреции большого количества бикарбоната в процессе образования НСl.
Под действием НСl происходит денатурация белков пищи, не подвергшихся термической обработке, что увеличивает доступность пептидных связей для протеаз. НСl обладает бактерицидным действием и препятствует попаданию патогенных бактерий в кишечник. Кроме того, соляная кислота активирует пепсиноген и создаёт оптимум рН для действия пепсина.
2.Механизм активации пепсина
Под действием гастринов в главных клетках желудочных желёз стимулируются синтез и секреция пепсиногена – неактивной формы пепсина. Пепсиноген – белок, состоящий из одной полипептидной цепи с молекулярной массой 40 кД. Под действием НСl он превращается в активный пепсин (молекулярная масса 32,7 кД) с оптимумом рН 1,0-2,5. В процессе активации в результате частичного протеолиза от N-конца молекулы пепсиногена отщепляются 42 аминокислотных остатка, которые содержат почти все положительно заряженные аминокислоты, имеющиеся в пепсиногене. Таким образом, в активном пепсине преобладающими оказываются отрицательно заряженные аминокислоты, которые участвуют в конформационных перестройках молекулы и формировании активного центра. Образовавшиеся под действием НСl активные молекулы пепсина быстро активируют остальные молекулы пепсиногена (аутокатализ). Пепсин в первую очередь гидролизует пептидные связи в белках, образованные ароматическими аминокислотами (фенилаланин, триптофан, тирозин) и несколько медленнее – образованные лейцином и дикарбоновыми аминокислотами. Пепсин – эндопептидаза, поэтому в результате его действия в желудке образуются более короткие пептиды, но не свободные аминокислоты.
Соседние файлы в предмете Биохимия
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
Источник
ПЕПСИН – основной протеолитический фермент желудочного сока (КФ 3.4.23.1), относится к группе пептид-гидролаз, расщепляет белки, в основном до полипептидов, хотя среди продуктов расщепления белков пепсином встречаются низкомолекулярные пептиды и аминокислоты. Препараты П. используют в качестве лекарственных средств для заместительной терапии при расстройствах пищеварения. При нек-рых патол, состояниях активность П. в желудочном соке (см.) является одним из диагностических признаков и определяется в клинико-биологических лабораториях. Содержание профермента П. – пепсиногена в моче (уропепсина) – служит дополнительным диагностическим тестом при исследовании секреторной способности слизистой оболочки желудка. П. находит применение в пищевой и мясо-молочной промышленности.
П. открыт в 1836 г. Т. Шванном, а в 1930 г. получен Нортропом (J. Н. Northrop) в кристаллическом виде.
П. является наиболее хорошо изученным представителем подкласса карбоксильных протеиназ (см. Пептид-гидролазы). Мол. вес (масса) П. ок. 35 000, изоэлектрическая точка (см.) находится при pH ниже 1,0, что обусловлено высоким содержанием в молекуле фермента остатков аспарагиновой и глутаминовой к-т при низком содержании диаминокислот, а также присутствием одного остатка фосфорной к-ты. Молекула П. состоит из одиночной полипептидной цепи из 327 аминокислотных остатков и представляет собой глобулу с размерами осей 5,5 X 4,5 X 3,2 нм, составленную из двух доменов, имеющих сходную структуру. Для молекулы П. характерно очень низкое содержание альфа-спиральных участков и высокое содержание бета-структур. Между доменами находится впадина, в к-рой располагается активный центр П., он формируется аминокислотными остатками, локализованными в разных доменах; каталитическими группами являются COOH-группы остатков аспарагиновой к-ты в 32-м и 215-м положениях.
Активность П., как и других карбоксильных протеиназ, подавляется диазокарбонильными ингибиторами и нек-рыми эпоксидами, специфически блокирующими COOH-группы активного центра фермента. Природным ингибитором П. является пепстатин – N-замещенный пентапептид, продуцируемый нек-рыми стрептомицетами.
П. наиболее устойчив при pH ок. 5,0-5,5. В более кислой среде происходит самопереваривание (аутолиз) фермента; при pH выше 6,0 наступает его быстрая и практически необратимая инактивация. П. инактивируется также при температуре выше 60°.
П. содержится в желудочном соке млекопитающих, птиц, рептилий и рыб. У беспозвоночных и микроорганизмов обнаружены ферменты, близкие по свойствам к П. В желудочном соке человека и высших млекопитающих наряду с П. присутствует гастриксин – фермент, имеющий сходные с П. свойства и гомологичную структуру.
Синтезируется П. главными клетками желез слизистой оболочки желудка (см.) в виде неактивного предшественника – профермента пепсиногена, к-рый в присутствии соляной к-ты желудочного сока превращается в активный фермент. При этом в результате конформационных изменений и гидролиза пептидной связи между лей44-иле45 от N-концевого участка молекулы пепсиногена отщепляется фрагмент, и т. о. образуется активный П., катализирующий затем аутокаталитическую активацию следующих порций профермента. Один из отщепляющихся при этом пептидов, так наз. ингибитор П. с мол. весом (массой) ок. 3000, при pH выше 5,0 подавляет активность П.; при pH ниже 4,0 ингибитор быстро расщепляется. В моче млекопитающих, в т. ч. и человека, в норме обнаруживается пепсиноген (уропепсин), проникающий в мочу из главных клеток слизистой оболочки желудка через кровь и почки (см. Уропепсин).
Процесс переваривания белков в жел.-киш. тракте начинается с действия П. Этот фермент обладает широкой субстратной специфичностью; он катализирует в белках гидролиз пептидных связей, образованных различными аминокислотными остатками. П. расщепляет почти все белки растительного и животного происхождения, за исключением протаминов и кератинов. Оптимум действия П. при pH 2,0. При pH ок. 5,0 П. створаживает молоко, вызывая превращение казеиногена в казеин (см.). П. способен гидролизовать ряд низкомолекулярных синтетических пептидов и эфиров, в состав к-рых входят ароматические аминокислоты. Оптимум для гидролиза П. многих синтетических субстратов находится при pH 4,0. П. катализирует также реакцию транс-пептидирования (перенос аминокислотного остатка с одного синтетического субстрата на другой).
Коммерческие препараты неочищенного П. получают из кислотного экстракта (аутолизата) слизистой оболочки желудка путем высаливания 15% р-ром NaCl и последующего высушивания. Очищенный П. выделяют из таких препаратов с помощью ионообменной хроматографии ( см.). Аналог П. – химозин (см.), используемый в пищевой промышленности для сыроварения, получают таким же способом из слизистой оболочки сычуга – отдела желудка крупного рогатого скота. Для мед. целей применяют П. из слизистой оболочки желудка свиней. Кристаллический П. может быть получен как из коммерческих препаратов П., так и из желудочного сока или непосредственно из слизистой оболочки желудка.
Для определения активности П. предложено много методов. Ранее использовали метод Метта, к-рый, однако, устарел и не дает точных результатов. Наиболее часто для определения активности П. применяют метод Ансона – расщепление под действием П. денатурированного гемоглобина с последующим определением количества тирозина в без-белковом фильтрате (см. Ансона – Черникова метод). Для исследования активности П. в желудочном соке и содержания уропепсина в моче широко применяется метод Пятницкого, основанный на определении створаживающей активности фермента.
При ряде заболеваний жел.-киш. тракта – хрон, гастрите (см.), язве желудка и двенадцатиперстной кишки (см. Язвенная болезнь), раке желудка (см.) и при нек-рых патол, состояниях – пернициозной анемии (см.), гипохромной анемии (см. Железодефицитная анемия) нарушается секреция П. В связи с этим определение П. в желудочном соке наряду с определением концентрации соляной к-ты имеет диагностическое значение. Для диагностических целей используют также определение в моче уропепсина, содержание к-рого, как полагают, отражает уровень секреторной способности слизистой оболочки желудка.
См. также Ферменты.
Пепсин как лекарственный препарат
Препарат П. (Pepsinum), используемый как лекарственное средство, получают из слизистой оболочки желудка свиней, в качестве наполнителя применяют сахарозу или лактозу. Препарат представляет собой белый или кремовый порошок сладкого вкуса со специфическим запахом, растворимый в воде, в 20% этиловом спирте и нерастворимый в эфире и хлороформе.
Обычно препараты П. обладают довольно низкой протеолитической активностью: 1 г препарата содержит всего 5 мг чистого фермента.
Для обеспечения оптимального действия препарата реакция среды в желудке должна быть кислой, а концентрация свободной соляной к-ты – не ниже 0,15-0,2%.
П. применяют для заместительной терапии при расстройствах пищеварения (см.), сопровождающихся секреторной недостаточностью желудка (ахилии, гипацидных и анацидных гастритах, диспепсиях и др.). Следует учитывать, что эндогенный П., как и другие пищеварительные ферменты, главные клетки слизистой обрлочки желудка выделяют обычно в избыточных количествах, поэтому снижение переваривающей способности желудочного сока при снижении его кислотности часто является результатом недостаточного выделения соляной к-ты, а не снижения активности или интенсивности образования П. Т. о., при гипацидных состояниях основное значение имеет обеспечение оптимальных условий для переваривания желудочного содержимого, а применение П. имеет вспомогательное значение. При анацидных состояниях, когда снижена кислотообразующая функция желудка, целесообразно назначать П. в сочетании с разведенной соляной к-той.
П. назначают внутрь: взрослым по 0,2-0,5 г на прием 2-3 раза в день перед едой или во время еды в порошках или в 1-3% р-ре соляной к-ты (10-15 капель на полстакана воды); детям на прием назначают по 0,05-0,3 г в 0,5-1% р-ре соляной к-ты. Противопоказаниями к приему П. являются гиперацидный гастрит, обострение при язве желудка. Побочным действием препарат, применяемый в терапевтических дозах, не обладает.
Форма выпуска: порошок. Хранение: в хорошо укупоренных банках в прохладном (от 2 до 15°), защищенном от света месте.
Кроме препарата пепсина (Pepsinum), фармацевтическая промышленность выпускает препарат ацидин-пепсин (Acidin-pepsinum), содержащий 1 часть пепсина и 4 части бетаина гидрохлорида (см. Бетаины), к-рый в желудке гидролизуется с образованием свободной соляной к-ты (0,4 г бетаина соответствуют примерно 16 каплям разведенной соляной к-ты). Таблетки ацидин-пепсина (по 0,5 и 0,25 г) растворяют в половине стакана воды и принимают 3-4 раза в день во время еды.
За рубежом таблетки, содержащие П., выпускаются под названиями «Ацидол-пепсин», «Бетацид», «Аци-пепсол», «Пепсамин».
См. также Ферментные препараты.
Библиография: Андреева Н. С. и др. Рентгеноструктурный анализ пепсина, Молек. биол., т. 12, № 4, с. 922, 1978, библиогр.; Лобарева Л. С. и Степанов В. М. Карбоксильные протеиназы плесневых грибов, в кн.: Усп. биол, хим., под ред. Б. Н. Степаненко, т. 19, с. 83, М., 1978, библиогр.; Мосолов В. В. Протеолитические ферменты, с. 101 и др., М., 1971; Нортроп Д., Кунитц М. и Херриотт Р. Кристаллические ферменты, пер. с англ., с. 32, М., 1950; Радбиль О. С. Фармакологические основы лечения болезней органов пищеварения, с. 78, М., 1976; Acid proteases, structure, and biology, ed. by J. Tang, N. Y., 1977; Tang J. Evolution in the structure and of carboxyl proteases, Molec, cell. Biochem., v. 26, p. 93, 1979.
Л. А. Локшина; H. В. Коробов (фарм.).
Источник
белка в целом. Именно поэтому денатурированные нагреванием белки (т.е. подвергшиеся термообработке мясные и рыбные продукты, вареные яйца), а также белки, набухшие под действием соляной кислоты желудочного сока, перевариваются значительно эффективнее, чем белки нативные, хотя при этом их первичная структура остается одинаковой. Протеиназы, входящие в состав желудочного, поджелудочного и кишечного соков воздействуют на пептидные связи в различных участках полипептидных цепей. Поэтому, только в результате комбинированного воздействия всего комплекса протеолитических ферментов желудочно-кишечного тракта осуществляется гидролиз белков до конечных продуктов, представленных свободными аминокислотами, а также ди- и трипептидами, которые всасываются эпителиальными клетками тонкого кишечника.
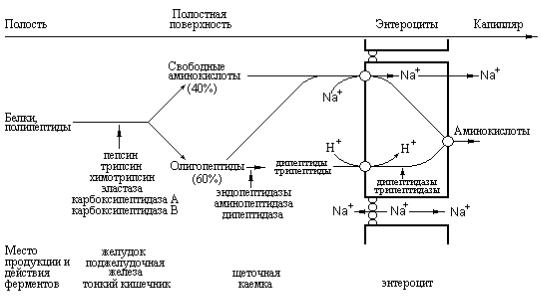
Рис. 2.3 Схема, отражающая последовательные стадии расщепления белков до аминокислот, ди- и трипептидов в желудочно-кишечном тракте (Textbook of Biochemistry with clinical correlations, Devlin T.M., (ed.), WILEY-LISS, 1993).
Таким образом, как показано на рис. 2.3, процесс переваривания белков может быть условно разделен на желудочную, панкреатическую и интестинальную фазы, в зависимости от участия тех или иных протеиназ, имеющих соответствующее происхождение.
Хорошо известно, что в полости рта белки никаким изменениям не подвергаются вследствие отсутствия в слюне протеолитических ферментов. Переваривание белков начинается в желудке. Выделяют три основных фактора, обеспечивающих инициацию процесса переваривания:
−стимуляция выделения гастрина присутствием белка пищи в желудке;
−в свою очередь гастрин обеспечивает секрецию обкладочными клетками слизистой желудка соляной кислоты;
−секреция пепсиногена главными клетками слизистой желудка.
Желудочный сок характеризуется присутствием высокой концентрации HCl и, следовательно, низким значением рН (рН ≈ 2.0), а также наличием протеиназ семейства пепсина. Высокая кислотность содержимого желудка имеет чрезвычайно важное физиологическое и биохимическое значение:
−во-первых, сильно кислая среда обеспечивает набухание и денатурацию пищевых белков. При этом глобулярные белки утрачивают третичную структуру, вследствие чего внутренние петидные связи становятся доступными для действия протеиназ;
−во-вторых, присутствие соляной кислоты обеспечивает инициацию аутокаталитического процесса превращения пепсиногена в пепсин и создает оптимальные условия для проявления его протеолитической активности. Так, оптимальное значение pH желудочного сока для нормального функционирования пепсина человека составляет 1,5-2,5. При pH 5-6 пепсин практически не проявляет протеолитической активности.
−наконец, высокая концентрация соляной кислоты препятствует развитию
вполости желудка микрофлоры, действуя как антисептик, тем самым, предотвращая зарождение гнилостных процессов. Хорошо известно, что при гастритах, при недостаточной кислотности желудочного сока гнилостные процессы в желудке являются причиной появления у больных неприятного запаха изо рта.
Влабораторной клинической практике для тестирования состояния желудка обычно определяют как «свободную» соляную кислоту, так и общую кислотность желудочного сока. Для этого, определенный объем желудочного сока титруют 0,1 N раствором щелочи в присутствии индикаторов – фенолфталеина для определения общей кислотности и диметиламидоазобензола при определении свободной HCl. Область перехода окраски фенолфталеина лежит в пределах pH 8,2-10,0, что позволяет определить всю совокупность кисло реагирующих веществ (свободная HCl, кислота, связанная с белками, фосфаты, органические кислоты и др.) в желудочном соке.
Диметиламидоазобензол изменяет окраску в пределах значений pH 2,4-4,0. Эта область pH соответствует моменту нейтрализации щелочью практически всей свободной HCl. Кислотность желудочного сока выражают
вмиллилитрах 0,1N раствора NaOH, расходуемого на титрование 100 мл сока – титрационных единицах.
При нормальной функции желудка общая кислотность колеблется обычно в пределах 40-60 титрационных единиц, а свободная соляная кислота
-20-40 единиц.
Внастоящее время разработаны беззондные методы определения кислотности желудочного сока. Суть этих методов состоит в использовании ионообменных смол с присоединенным хинином. При введении такой смолы
вполость желудка соляная кислота связывается с катионитом, вытесняя хинин, который всасывается в кровь и выводится из организма с мочой. По количеству выделившегося хинина судят о содержании HCl в желудочном соке.
Действие пепсина
Важнейшую роль в переваривании белков в желудке играет протеиназа – пепсин, который секретируется главными клетками слизистой желудка в каталитически неактивной форме – в виде пепсиногена. Активный пепсин образуется из предшественника – пепсиногена (мол. масса 40.000 дальтон) при удалении 44 аминокислотных остатков с N-конца белковой молекулы. Расщепление пептидной связи между аминокислотными остатками в положениях 44 и 45 в пепсиногене может происходить либо посредством автоактивации внутримолекулярной реакции гидролиза при рН ниже 5.0, либо в присутствии следов пепсина за счет автокатализа. Освобождающийся N-концевой пептид остается связанным с остальной частью молекулы фермента и действует как ингибитор пепсина при рН выше 2.0. Этот ингибирующий эффект устраняется либо при снижении рН до значений меньших 2.0, либо в результате дальнейшей деградации N- концевого пептида под действием пепсина. Далее образовавшийся пепсин активирует другие молекулы пепсиногена и весь процесс приобретает лавинообразный характер.
Пепсины являются уникальными белками хотя бы потому, что чрезвычайно устойчивы к действию кислот. Фактически эти протеиназы активны только в сильно кислой среде и не активны при нейтральном значении рН. Механизм катализа зависит от присутствия в активном центре фермента двух карбоксильных групп, принадлежащих двум остаткам аспарагиновой кислоты, причем одна карбоксильная группа находится в ионизованной форме, а другая в недиссоциированном состоянии. По этой причине пепсины относят к семейству карбоксипротеиназ. Характерной особенностью карбоксипротеиназ является их ингибирование пепстатином,
который оказывает ингибирующее действие в очень низких концентрациях, порядка 10-10 М.
Основной желудочной протеиназой является пепсин А (мол. масса 33.000 дальтон), который преимущественно расщепляет пептидные связи,
образованные аминогруппами ароматических аминокислот – тирозина,
фенилаланина и триптофана, а также связи Ala-Ala и Ala-Ser. Нервнорефлекторные механизмы отделения желудочного сока и
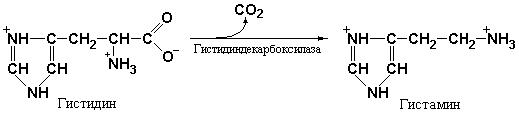
регуляция желудочной секреции достаточно подробно рассматриваются в курсах физиологии. Тем не менее, необходимо остановиться на некоторых аспектах действия гуморальных факторов. К числу таких факторов относится гистамин, являющийся продуктом декарбоксилирования аминокислоты гистидина под действием гистидин-декарбоксилазы (рис. 2.4) и «пищеварительный» гормон гастрин, выполняющий наиболее важную роль в стимуляции секреции желудочного сока. Образование гастрина в слизистой оболочке привратника желудка и поступление его в кровь резко усиливается при поступлении в желудок пищи.
Рис. 2.4 Гистамин является продуктом декарбоксилирования аминокислоты гистидина под действием гистидин-декарбоксилазы
Сравнение активностей этих двух факторов показывает, что полипептид гастрин обладает в 500 раз более высокой способностью стимулировать функцию желудка, чем гистамин. Однако, при введении человеку даже 1 мг гистамина в кровь, обнаруживается интенсивное отделение желудочного сока. Подобная гистаминовая проба используется в лабораторной клинической практике для дифференциальной диагностики ахилий – патологических состояний, характеризующихся неспособностью желудка секретировать пепсин и HCl. Отсутствие секреции в ответ на введение гистамина свидетельствует об атрофическом изменении слизистой желудка. В ходе активации пепсина не весь пепсиноген принимает участие в этом процессе. Частично пепсиноген всасывается в кровь, доставляется в почки и переходит в состав мочи. Присутствующий в моче пепсиноген получил специальное название уропепсиногена. В клинических лабораториях, особенно в педиатрической практике, часто определяется активность уропепсиногена (уропепсина) для оценки функционального состояния и секреторной функции слизистой желудка у детей. При пониженной секреции желудочного сока и при наличии атрофических процессов активность уропепсина резко снижается, а при гиперсекреторных состояниях, например при язвенной болезни – повышается.
В клинической практике определяют также активность пепсина, особенно при отсутствии свободной HCl в желудочном соке. Это позволяет отличать анацидные состояния (отсутствие HCl при наличии пепсина) от истинных ахилий, при которых секреция желудка практически отсутствует.
Основными продуктами гидролиза белка под действием пепсина являются большие пептидные фрагменты и некоторое количество свободных аминокислот. Значение переваривания белков в желудке сводится, в первую очередь, к появлению пептидов и аминокислот, которые действуют в качестве стимуляторов синтеза и выброса холецистокинина. Поэтому пептиды, образованные в результате гидролитического расщепления пищевых белков под действием желудочных протеиназ, являются инструментом инициации панкреатической фазы переваривания белка.

Лекция № 3
Переваривание белков в тонком кишечнике. Активация панкреатических зимогенов
Как только кислое содержимое желудка попадает в тонкий кишечник, в нем под влиянием низкого pH начинается секреция гормона секретина, поступающего в кровь. Секретин, в свою очередь стимулирует выделение поджелудочной железой бикарбоната, что приводит к нейтрализации HCl желудочного сока. В результате pH резко возрастает от 1,5-2,5 до ~7,0. При нейтральном значении pH в тонком кишечнике продолжается переваривание белков под действием протеиназ поджелудочной железы. Секреция этих протеиназ стимулируется гормоном холецистокинином, продукция которого зависит от поступления в двенадцатиперстную кишку свободных аминокислот.
Пищеварительный сок поджелудочной железы содержит большое количество проэнзимов эндопептидаз и карбоксипептидаз. Эти зимогены активируются только после того, как попадут в просвет тонкого кишечника. Ключевым ферментом, ответственным за их активацию, является энтерокиназа – протеиназа, продуцируемая эпителиальными клетками двенадцатиперстной кишки. Энтерокиназа активирует панкреатический трипсиноген посредством отщепления гексапептида NH2 – Val – (Asp)4 – Lys с N-конца этого зимогена, превращая его тем самым в активный трипсин
(рис. 3.1).
Рис. 3.1 Схема, иллюстрирующая процесс активации трипсина под действием энтерокиназы.
Далее активный трипсин способен автокаталитически активировать другие молекулы трипсиногена. Более того, трипсин также действует на другие проэнзимы такие, как химотрипсиноген, проэластаза и прокарбоксипептидазы А и В (рис. 3.2). Поскольку трипсин играет роль общего мощного активатора панкреатических пищеварительных ферментов, в соке поджелудочной железы присутствует низкомолекулярный пептид,
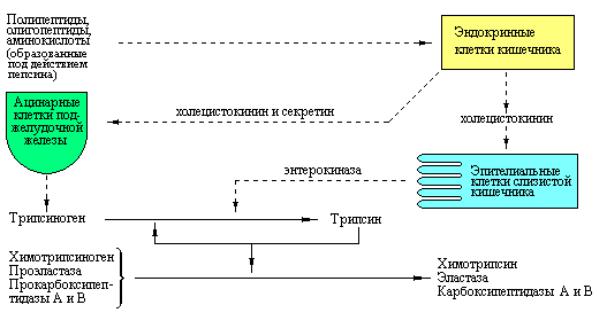
действующий как ингибитор трипсина и предотвращающий преждевременную активацию тех незначительных количеств трипсина, которые могут оказаться в клетках поджелудочной железы или ее протоках.
Рис. 3.2 Схема, иллюстрирующая последовательность стадий секреции и активации панкреатических ферментов.
Субстратная специфичность трипсина, химотрипсина и эластазы – основных панкреатических эндопептидаз – указана в табл. 3.1. Панкреатические протеолитические ферменты активны только при значениях рН, близких к нейтральному, поэтому эффективность их каталитического действия зависит, как было указано выше, от секреции бикарбоната, нейтрализующего соляную кислоту желудочного сока. Перечисленные выше эндопептидазы относят к семейству сериновых протеиназ, содержащих в активных центрах специфический остаток серина (у химотрипсина это Ser-195), ответственный за протеолитическую активность ферментов. Характерной особенностью сериновых протеиназ является их способность необратимо ингибироваться при действии органических фторфосфатов, конкретнее, при взаимодействии остатка активного серина с диизопропилфторфосфатом (см. далее).
Полипептиды и олигопептиды, образованные в результате протеолиза под действием пепсина и панкреатических эндопептидаз, подвергаются дальнейшей деградации в просвете тонкого кишечника при участии карбоксипептидаз А и В. Эти белки являются металлоферментами, для проявления активности которых необходимо присутствие в активном центре атома Zn и, следовательно, механизм их действия должен отличаться от механизма катализа карбокси- и сериновых протеиназ.

В результате комбинированного действия панкреатических пептидаз образуются свободные аминокислоты и короткие пептиды, состоящие из 2-8 аминокислотных остатков. Пептиды, образующиеся на данной стадии переваривания пищевого белка, содержат до 60% аминного азота.
Участие пептидаз тонкого кишечника в расщеплении коротких пептидов
Поскольку секрет поджелудочной железы не содержит каких-либо заметных количеств аминопептидаз, окончательное переваривание олиго- и дипептидов зависит от функционирования ферментов щеточной каемки тонкого кишечника. Полостная поверхность плазматических мембран эпителиальных клеток кишечника особенно богата ферментами, проявляющими эндопептидазную и аминопептидазную активности, а также содержит дипептидазы с различной субстратной специфичностью. Конечными продуктами процесса пристеночного пищеварения являются свободные аминокислоты, ди- и трипептиды. Аминокислоты и короткие пептиды способны всасываться эпителиальными клетками при помощи специфических транспортных систем. Поступающие в энтероциты ди- и трипептиды гидролизуются в цитоплазме этих клеток до аминокислот и только после этого покидают клетки, направляясь в кровяное русло. Присутствие в цитоплазме эпителиальных клеток кишечника дипептидаз объясняет появление в воротной вене (после принятия пищи) практически только свободных аминокислот.
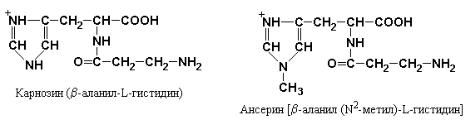
Фактическое отсутствие пептидов в крови ранее служило доказательством того, что при полостном пищеварении происходит полный гидролиз белков пищи до свободных аминокислот. Однако в настоящее время установлено, что большая часть аминного азота пищи всасывается в виде простейших пептидов, которые гидролизуются внутриклеточно. Исключение из этого общего правила составляют ди- и трипептиды, содержащие пролин или оксипролин, а также включающие необычные аминокислоты такие, как β-Аlа в карнозине (β-аланилгистидине) и ансерине [β-аланил (N2-метил) гистидине], присутствующие в мясе цыплят.
Дипептиды карнозин и ансерин являются «плохими» субстратами для дипептидаз цитоплазмы энтероцитов и поэтому транспортируются в неизмененном виде из эпителиальных клеток кишечника в кровяное русло.
Источник
